在肿瘤创新药研发中,G蛋白偶联受体(GPCR)一直是一个有些尴尬的靶点家族。从成药史来看,它是最成熟的一类药物靶点;但从肿瘤新药版图来看,GPCR又长期没有HER2、TROP2、CLDN18.2这类靶点那么显眼。
不过,从AACR 2026的摘要趋势来看,这种局面正在发生变化。本届会议上,GPCR相关项目已经明显从传统小分子受体调控,延伸到肿瘤微环境、Treg清除、ADC、双抗、多特异性分子以及放射性药物等多个方向。尤其是CXCR4、SSTR2、CCR8、LGR5、GPRC5D、CCR5等靶点,不仅摘要露出相对集中,而且已经出现较清晰的产品化和平台化开发路径。
1、CXCR4:成熟靶点仍在迭代,转移与微环境价值持续放大
在GPCR靶点中,CXCR4依然是最成熟、也最接近临床转化的一类。它在肿瘤中的价值主要围绕细胞迁移、骨髓归巢、转移、耐药和微环境重塑展开,因此既有基础研究深度,也有较强的临床延展性。AACR 2026上,CXCR4的关注点已经从“做不做这个靶点”进一步转向为“如何做患者分层、如何进入联合治疗,以及如何挖掘更明确的应答人群”。
从本届摘要来看,CXCR4方向既有Motixafortide这类明确分子的临床转化信号,也有TNX-1700这样的新项目线索,说明这一靶点仍然处于持续活跃状态。代表性摘要包括:

2、SSTR2:从核药标杆靶点,走向更广义的偶联平台靶点
在GPCR家族中,SSTR2是最具“核药属性”的代表靶点之一。过去提到SSTR2,首先想到的通常是神经内分泌肿瘤和放射配体治疗;但AACR 2026显示,这个靶点的开发边界正在快速拓宽,已经不再局限于传统的显像或核素治疗,而是明显延伸到肽偶联药物、双特异性ADC以及新型放射性偶联药物。从布局主体看,Italfarmaco、基石药业、上海核舟医药都带来了明确项目线索,说明SSTR2正在从“经典核药靶点”逐步演变成一个更广义的偶联递送平台靶点。代表性摘要包括:

3、CCR8:Treg清除赛道持续升温,免疫抑制微环境成为核心切口
如果说本届AACR上哪个GPCR靶点最能体现“肿瘤免疫新方向”,那CCR8一定是重点之一。CCR8与肿瘤浸润性调节性T细胞(Treg)高度相关,因此天然适合作为肿瘤免疫抑制微环境改造的切入点。相比传统免疫激活逻辑,CCR8更强调定向清除肿瘤相关Treg,这也是它快速升温的重要原因。
从今年AACR的摘要看,CCR8已经出现较完整的开发梯队:既有去除型抗体的分子特征研究,也有一期临床结果,甚至开始向ADC方向延展。布局主体包括Kainova Therapeutics、Amgen、Takeda,产业化信号已经比较明确。代表性摘要包括:

4、LGR5:从肿瘤干细胞标志物,走向ADC与双抗开发靶点
LGR5是一个典型的“生物学意义先行、药物开发逐步跟上”的靶点。它长期与肿瘤干细胞、耐药和复发相关,因此早年更多出现在机制研究中。但从AACR 2026的信号来看,LGR5正在快速摆脱“只适合做文章”的印象,转向更实在的抗体药物开发阶段。这次会议里,LGR5方向已经出现LGR5靶向ADC、EGFRxLGR5双抗、VHH抗体等多种策略,说明它正在成为实体瘤中值得重新评估的可药物化靶点。企业层面,Dragon Boat Biopharmaceutical的项目推进最为直接。代表性摘要包括:

5、GPRC5D:骨髓瘤赛道里最具热度的GPCR靶点之一
在血液瘤领域,GPRC5D已经成为继BCMA之后极具关注度的新一代靶点之一。尤其是在多发性骨髓瘤中,GPRC5D为复发难治患者提供了新的靶向维度,也因此成为多特异性抗体和T-cell engager开发中的重点对象。AACR 2026上,这一靶点已经不再只是概念验证,而是明显进入了平台竞争与分子设计优化阶段。
从摘要看,GPRC5D方向既有Talquetamab相关临床应用背景,也有多特异性抗体和多价多特异性ADC的新设计。相关布局主体包括Integral Molecular和Synthetic Design Lab,显示这一靶点正在进入“谁能做得更优”的竞争阶段。代表性摘要包括:

6、CCR5:老靶点正在被重新激活,联合治疗价值值得重估
和前面几个靶点相比,CCR5并不是一个“新方向”。它在炎症、病毒感染和免疫迁移领域早已被广泛研究,因此很多人对它的第一印象甚至不是肿瘤。但AACR 2026的一些摘要提示,CCR5在肿瘤中的开发空间远未被挖尽,尤其是在联合治疗、微环境调控和适应症拓展上仍有不少机会。
这次会议中,CCR5相关线索主要围绕leronlimab和maraviroc等已有分子的再利用展开,体现出典型的“老靶点新场景”特征。对于希望寻找机制成熟、转化路径相对清晰的团队来说,CCR5仍然值得持续关注。代表性摘要包括:

7、CXCR2:肿瘤炎症轴的关键节点,适合与免疫和微环境策略联动
在本届AACR中,CXCR2的摘要数量不算最多,但研究方向非常集中,几乎都围绕IL-8、中性粒细胞募集、肿瘤炎症和休眠细胞唤醒展开。这类靶点的价值不在于单纯作用于肿瘤细胞,而在于它连接了肿瘤与髓系免疫系统之间的通讯网络,因此很适合与免疫治疗、炎症阻断和耐药微环境调控联动。从企业化线索看,虽然本次会议上披露的成熟项目不算多,但AZD5069等已有分子仍然给出了较明确的转化方向。代表性摘要包括:

8、DRD1:神经递质受体在肿瘤中的角色,正从边缘走向前沿
如果说前面的几个靶点已经更接近“产品开发逻辑”,那么DRD1更像是本届AACR中一个值得前瞻关注的信号。作为多巴胺受体家族成员,DRD1传统上并不属于肿瘤药物开发的核心靶点,但这次多篇摘要将其与EZH2、表观遗传调控和三阴性乳腺癌进展联系起来,提示神经递质信号和肿瘤表观遗传之间的交叉正在被重新认识。目前这一方向仍以前沿研究为主,产业化布局还不密集,但恰恰因为处于早期,更值得被持续跟踪。代表性摘要包括:

回看AACR 2026,可以非常明显地感受到,GPCR已经不再只是传统小分子药物的主场。在肿瘤领域,越来越多的GPCR靶点正在进入抗体、ADC、双抗、放射性药物和免疫微环境重塑的开发体系。其中,CXCR4、CCR8、CCR5、CXCR2更偏向免疫与微环境调控;SSTR2代表的是核药与偶联药物的持续融合;而LGR5、GPRC5D则更像是GPCR靶点走向抗体工程、多特异性分子和ADC开发的标志性案例。如果说过去行业对GPCR的判断还是“肿瘤里有机会,但不算主流”,那么从今年AACR的趋势看,至少一部分GPCR靶点,已经开始真正进入主流创新药视野。
缔码Nanodisc膜蛋白平台及现货GPCR抗体序列助力GPCR药物开发
纳米盘(Nanodisc),又称为纳米圆盘,在膜蛋白研究中具有不可替代的重要性,它有效解决了膜蛋白表达、纯化及功能检测中面临的诸多难题。Nanodisc可根据所使用的稳定剂类型进行分类,主要包括膜支架蛋白型(MSP Nanodiscs)、合成型(Polymer-based Nanodisc;Synthetic Nanodiscs)以及肽型(Peptide-based Nanodisc;PeptiNanodiscs)。缔码生物Nanodisc平台利用哺乳动物细胞表达系统生产重组膜蛋白,使其在结构和功能上尽可能接近天然状态,不仅提高了膜蛋白研究的成功率,也加快了新药靶点的筛选和候选药物分子的开发进程,为结构生物学研究及精准药物研发提供了坚实保障。目前,缔码生物在利用Synthetic Nanodiscs和PeptiNanodiscs已开发出500+全长多跨膜蛋白,覆盖GPCR及离子通道等多个热门药物靶点家族。
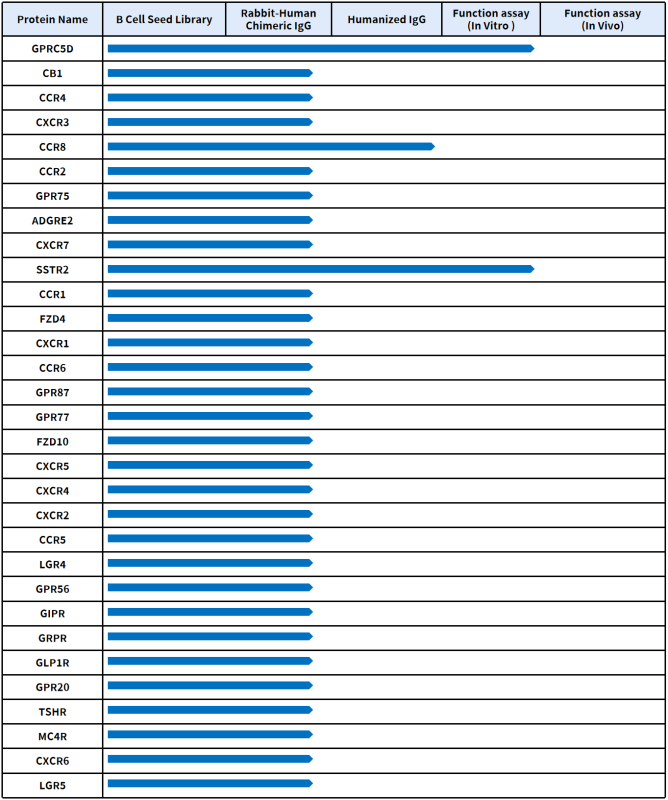
点击查看所有nanodisc产品此外,针对热门的GPCR及离子通道药物靶点,缔码生物已用其创新型B细胞抗体筛选平台获得多个功能抗体序列,客户第二天即可拿到序列进行功能测试更多详情,欢迎咨询。