近年来,代谢-免疫交叉成为药物研发的重要方向,其中G蛋白偶联受体84(G protein-coupled receptor 84,GPR84,又称为EX33)作为中链脂肪酸受体逐渐成为研究热点。最新研究表明,GPR84在免疫调控中具有多重作用:一方面可增强巨噬细胞吞噬功能并参与抗肿瘤免疫[1],另一方面又可通过激活NLRP3炎症小体放大炎症反应[2]。此外,近期研究还提示其可能参与肿瘤免疫微环境重塑及免疫治疗响应调控[3]。然而,与机制研究的快速进展相比,GPR84靶向药物的临床转化仍面临挑战,呈现出“机制明确但疗效不确定”的典型特征。那么,GPR84究竟具备怎样的结构特征?在体内如何发挥功能?又是通过哪些机制参与疾病发生,并能否真正成为可成药靶点?下面将逐一展开。
一、GPR84结构特点
人源GPR84是一类典型的Class A(rhodopsin-like)G蛋白偶联受体(GPCR),整体结构由7条跨膜α螺旋(TM1-TM7)构成,并通过胞外环(ECL1-3)和胞内环(ICL1-3)连接,形成经典的跨膜信号转导结构。其配体结合口袋位于TM3-TM7围成的中央腔体,呈现出明显的疏水性特征,这一结构基础决定了其对中链脂肪酸(如C10-C12)的高度选择性。
研究表明,该结合腔内部存在一个类似“链长筛选器”的疏水区域,可对脂肪酸碳链长度进行精细识别,从而限制过长或过短配体的结合能力。这种配体选择性机制与其他脂肪酸感知型GPCR具有一定共性。例如,FFAR1(GPR40)和FFAR4(GPR120)主要识别长链脂肪酸,而FFAR2(GPR43)和FFAR3(GPR41)则主要响应短链脂肪酸。相比之下,GPR84对中链脂肪酸(C9-C14)具有特异性识别能力,凸显其在连接脂质代谢与免疫调控中的独特作用。同时,受体中的关键残基R172通过静电作用稳定脂肪酸的羧基头部,形成“疏水尾部嵌入与极性头部锚定”的双重识别模式,这是GPR84配体识别的重要结构基础。
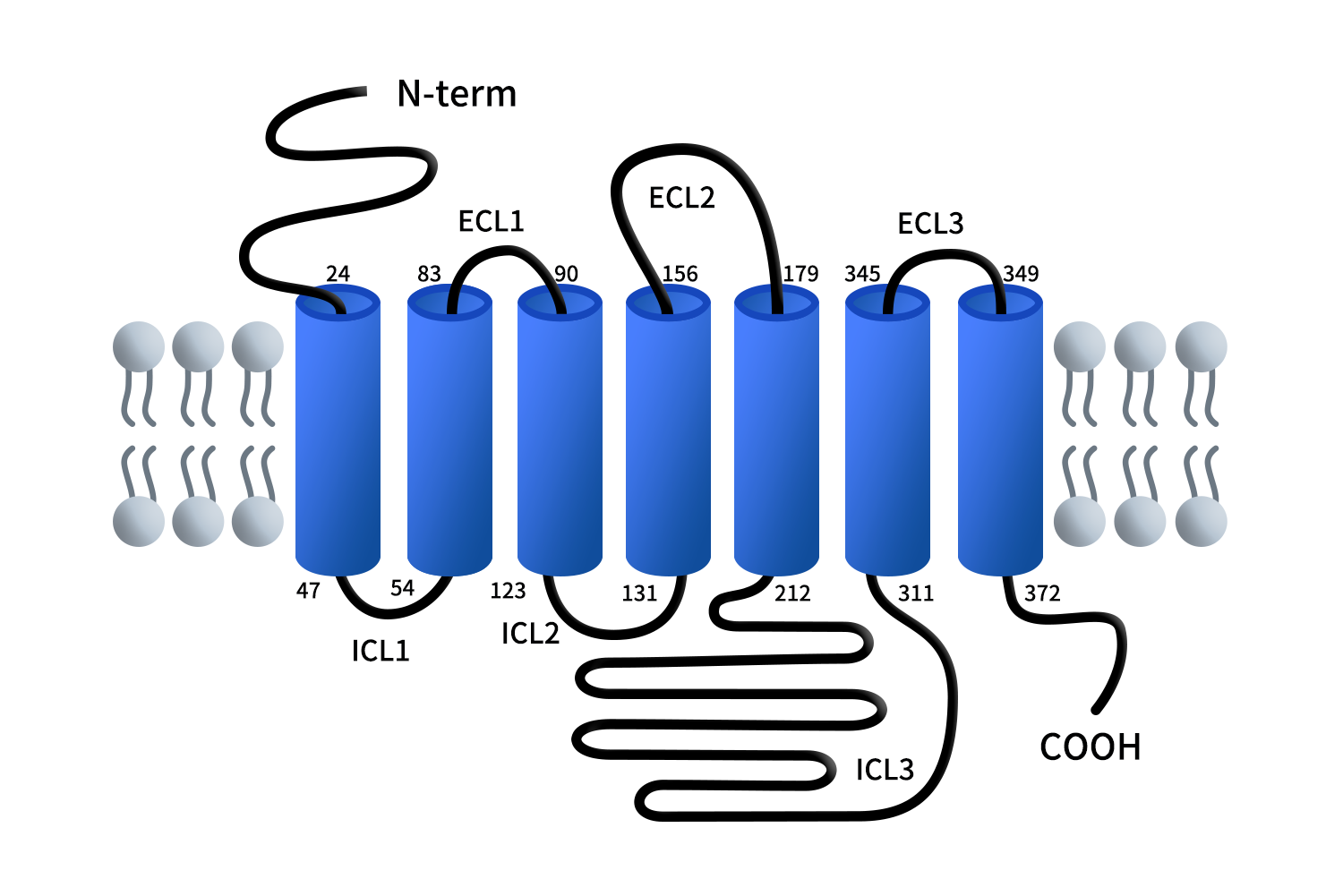
Figure 1. The structure of G protein-coupled receptor 84 (GPR84) [4]
此外,GPR84的胞外环2(ECL2)具有独特的构象特征,其整体向下覆盖配体结合口袋,既直接参与配体相互作用,又在空间上形成“门控结构”,调控配体进入受体内部。这一特征区别于多数GPCR中较为开放的配体进入路径,提示GPR84在配体识别过程中具有更高的结构选择性。在受体激活过程中,GPR84同样表现出典型GPCR特征,即跨膜螺旋TM6向外摆动以形成G蛋白结合界面,但其“微开关”机制具有一定特异性:传统GPCR中常见的W6.48(第6条跨膜螺旋上的第48位色氨酸)被Y6.48(第6条跨膜螺旋上的第48位酪氨酸)所替代,导致其激活过程中的氢键网络和构象变化模式有所不同,更依赖脂肪酸配体对疏水腔体的推动作用[4]。
二、GPR84的分布与生理功能
GPR84主要表达于免疫系统细胞,包括:中性粒细胞、单核细胞及巨噬细胞,其中在巨噬细胞中表达最为显著[5]。此外,在脂肪组织、肺组织及中枢神经系统(如小胶质细胞)中亦有一定表达[6]。GPR84可增强免疫细胞趋化、促进炎症因子释放并诱导活性氧(ROS)生成,从而放大炎症反应[8]。在巨噬细胞功能调控方面,研究表明,GPR84能够增强巨噬细胞吞噬作用[1]及促进M1型极化(促炎表型)[2]。此外,作为脂肪酸受体,GPR84可感知局部代谢状态变化,并将脂质信号转化为免疫响应,是典型的代谢-免疫连接节点[7]。
三、GPR84信号通路
GPR84作为典型的Gi蛋白偶联受体,中链脂肪酸(如癸酸、辛酸)[4]为其天然配体,其下游信号通路主要围绕炎症调控与免疫细胞活化展开。首先,在Gi-cAMP通路中,GPR84激活后通过Gi蛋白抑制腺苷酸环化酶(adenylate cyclase)活性,从而降低细胞内cAMP水平。由于cAMP通常具有抑制炎症反应的作用,其下降可解除对NF-κB等炎症通路的负调控,进而促进促炎细胞因子的表达与释放,增强免疫应答。
其次,GPR84可显著促进NLRP3炎症小体的激活。研究表明,其激活能够增强caspase-1活性,促进IL-1β和IL-18的成熟与分泌[2],从而在感染和组织损伤过程中放大炎症级联反应。这一通路在炎症性肠病及神经炎症等疾病中尤为关键。
此外,GPR84还可诱导Ca2+信号通路的激活,通过促进细胞内钙离子浓度升高,调控免疫细胞的趋化、黏附及吞噬功能。这种快速的离子信号变化有助于增强中性粒细胞和巨噬细胞对炎症刺激的响应能力。
四、GPR84相关疾病
GPR84在多种疾病中发挥关键作用,其功能与促炎特性密切相关。
4.1 炎症性疾病
在炎症性肠病(IBD)中,GPR84主要表达于肠道的单核细胞和巨噬细胞中。当局部中链脂肪酸浓度升高或免疫刺激存在时,GPR84被激活,从而增强NF-κB信号通路,促进促炎因子如IL-1β、TNF-α的分泌,加重肠道炎症反应[2]。动物实验显示,使用GPR84拮抗剂可显著降低炎症指标,缓解结肠病理损伤,提示其在IBD治疗中具有潜在应用价值。此外,在急性肺损伤(ALI)及感染性炎症中,GPR84通过调控中性粒细胞趋化和浸润,增强局部炎症反应[8]。过度活化则可能导致组织损伤,这也解释了其作为炎症“放大器”的双面角色。
4.2 纤维化与代谢疾病
GPR84在纤维化疾病中同样发挥重要作用。在特发性肺纤维化(IPF)及肝纤维化模型中,GPR84表达明显上调,与炎症因子及胶原沉积呈正相关[9]。通过促炎机制,GPR84可激活纤维化相关信号通路,如TGF-β/Smad,促进成纤维细胞增殖和胶原生成,推动组织纤维化的进展。这表明GPR84不仅是炎症放大器,也是纤维化的潜在驱动因子。
4.3 神经系统疾病
在中枢神经系统中,GPR84主要表达于小胶质细胞。其激活可促进NLRP3炎症小体组装,诱导IL-1β和IL-18释放,并触发细胞焦亡(pyroptosis),加重神经炎症和脑损伤[10]。这使得GPR84成为神经炎症及脑损伤相关疾病潜在干预靶点,尤其在卒中、脑外伤及神经退行性疾病中具有研究价值。
4.4 肿瘤
GPR84在肿瘤中的作用呈现明显“双重性”。一方面,它可增强巨噬细胞吞噬能力,提高肿瘤免疫监视和抗肿瘤效应[1];另一方面,在某些肿瘤微环境中,GPR84可促进巨噬细胞向免疫抑制型TAM(tumor-associated macrophages)极化,从而帮助肿瘤逃避免疫监视[4]。这种功能差异取决于肿瘤微环境中巨噬细胞的极化状态和局部代谢信号,提示在肿瘤治疗中需谨慎考虑GPR84靶向策略的时机和方式。
总体看来,GPR84通过调控炎症反应、纤维化进程、神经炎症以及肿瘤免疫微环境,形成一个广泛且多维度的疾病调控网络,既展示了其作为药物靶点的潜力,也凸显了开发策略的复杂性。
五、GPR84药物研发进展
不完全统计,目前全球针对GPR84的药物共计30款,其中10款处于临床前,10款处于药物发现,仅4款处于临床阶段。开发主要聚焦于小分子化药,用于治疗炎症和纤维化疾病。这里重点展示了临床阶段活跃的四款GPR84药物。

Setogepram (Fezagepras/PBI-4050)是Liminal BioSciences的第一代产品,是一款双靶点调节剂。它不仅是GPR84的拮抗剂,同时也是GPR40(FFAR1)的激动剂。目前处于临床3期,在阿尔斯特雷姆综合征(Alström syndrome)和特发性肺纤维化(IPF)中进行了广泛研究。虽然Setogepram证明了GPR84靶点在抗纤维化中的潜力,但由于其双靶点性质导致的复杂药理特性,Liminal后来转向了更具选择性的第二代拮抗剂(即LMNL-6511)。
LMNL-6511是一款新型、强效且具有口服生物利用度的GPR84选择性拮抗剂。实验数据表明,其体外效力比第一代药物高出约30倍。它通过精准靶向免疫细胞上的GPR84,干扰代谢-炎症轴,主要用于治疗非酒精性脂肪性肝炎(NASH/MASH)、炎症性肠病(IBD)和各类纤维化疾病,目前处于临床1/2期。在完成英国的I期随机双盲(SAD/MAD)研究并验证了良好的药代动力学(PK)特性后,Liminal于2025年启动了针对健康受试者的Ib期多剂量给药研究,以进一步评估其安全边界。2023年下半年,Structured Alpha LP完成了对Liminal BioSciences的溢价收购并将其退市,LMNL-6511作为其核心管线进入私有化开发阶段。
BGT-004 (604c)由泊及源(上海)生物医药开发,是一种具有对称磷酸二酯结构的GPR84拮抗剂。其作用机制集中于抑制中性粒细胞在肠道黏膜的浸润及活性氧(ROS)的产生,从而保护肠道屏障。临床前研究显示其在治疗溃疡性结肠炎(UC)方面具有显著的抗炎潜力,且能改善结肠损伤,目前处于临床I期(IND获批)。该药物已在中国获得临床试验许可,主要针对特应性皮炎(AD)和溃疡性结肠炎等免疫介导性疾病开展早期探索。
BAY-3178275由拜耳(Bayer,德国)开发,是一款小分子GPR84拮抗剂。与上述抗纤维化药物不同,拜耳将其主要应用方向定位在神经系统疾病。它通过调节神经炎症微环境中的小胶质细胞和髓系细胞活性,减轻因免疫代谢紊乱导致的神经损伤,目前处于临床I期(首次人体试验)。根据拜耳2025-2026年的管线披露,该药目前正在开展针对糖尿病周围神经病理性疼痛(DPNP)的安全性与初步疗效评估。
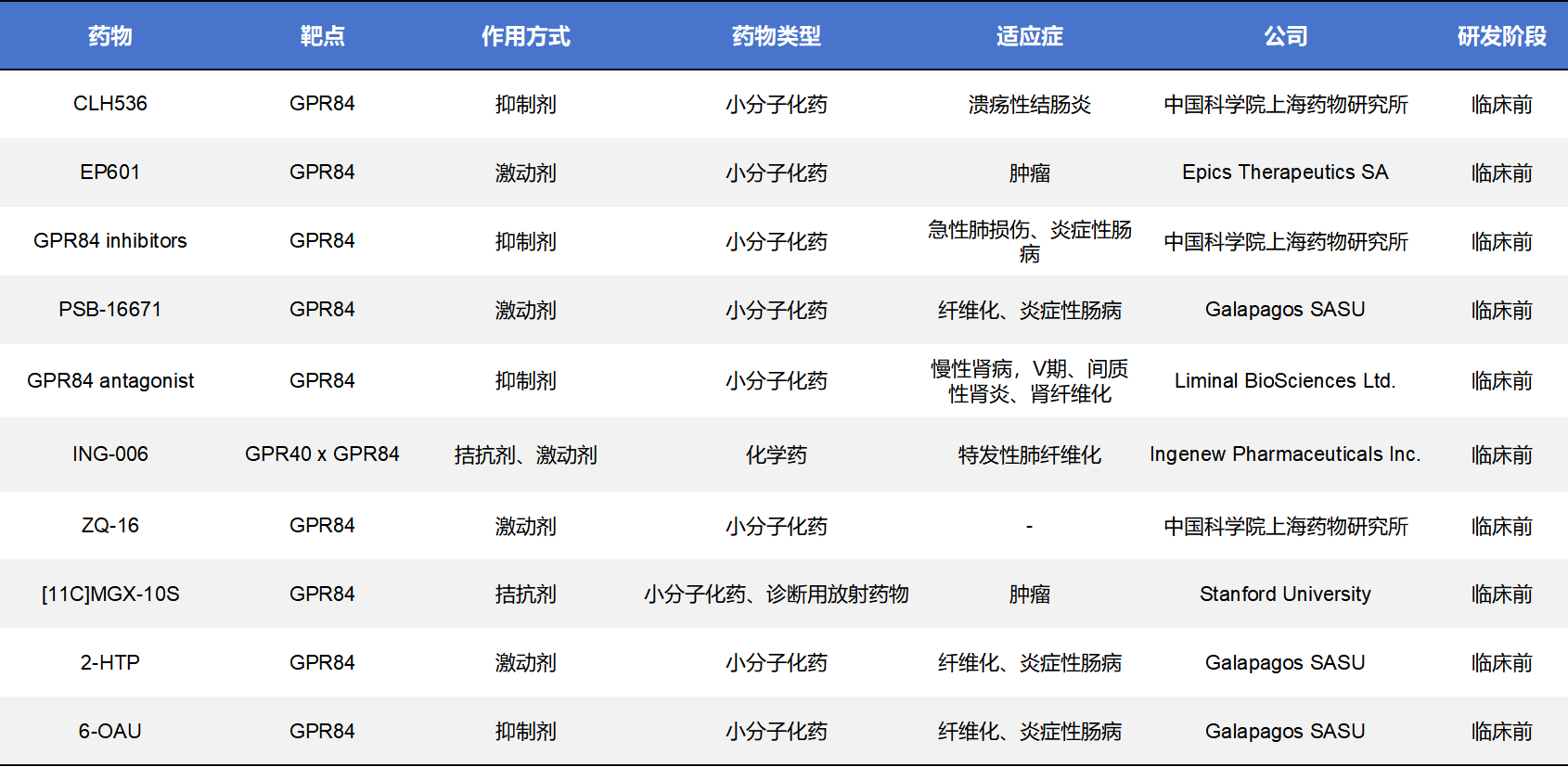
此外,临床前药物管线详情如下:
六、缔码生物GPR84 nanodisc助力GPR84靶向药物开发
如前所述,目前针对GPR84的药物开发主要还是集中在小分子药物,而在小分子药物的筛选过程中,GPR84的构象完整性直接觉得药物效果。由于全长GPR84结构复杂、跨膜区众多,传统可溶片段或细胞膜粗提物难以满足结构解析、结合位点验证及药筛需求。因此,能稳定呈现天然构象的GPR84 nanodisc全长膜蛋白,正成为开展机理研究与先导化合物评估的关键工具。
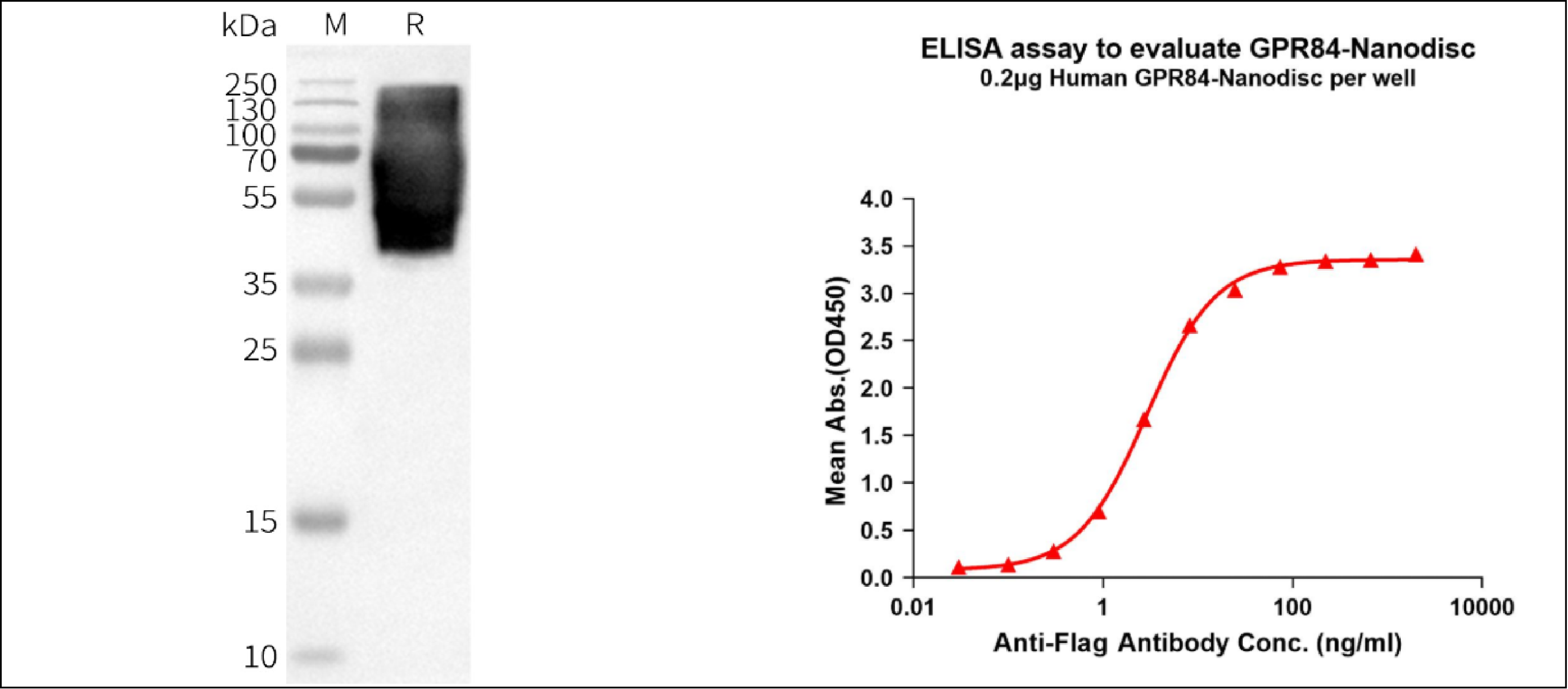
缔码生物利用其哺乳动物细胞表达系统已成功制备了具有天然构象与完整跨膜结构的全长 GPR84,该蛋白可在无去垢剂环境中保持天然构象与翻译后修饰,为结构分析、抗体筛选与药物结合测试提供更可靠的靶点模型,正逐渐成为药物研发早期的重要资源。
Human GPR84 full length protein-synthetic nanodisc (FLP100129)
| Target | Cat.No. | Product Name |
| GPR84 | FLP100129 | Human GPR84 full length protein-synthetic nanodisc In Stock |
| FLP120129 | Human GPR84-Strep full length protein-synthetic nanodisc | |
| PME101470 | Human GPR84 Protein, hFc Tag In Stock | |
| FFAR1/GPR40 | FLP100134 | Human FFAR1 full length protein-synthetic nanodisc In Stock |
| FLP120134 | Human FFAR1-Strep full length protein-synthetic nanodisc | |
| FFAR2/GPR43 | FLP120236 | Human FFAR2-Strep full length protein-synthetic nanodisc In Stock |
| FFAR3/GPR41 | FLP120237 | Human FFAR3-Strep full length protein-synthetic nanodisc In Stock |
| PME101912 | Human FFAR3 Protein, hFc Tag In Stock | |
| FFAR4/GPR120 | FLP100238 | Human FFAR4 full length protein-synthetic nanodisc In Stock |
| FLP120238 | Human FFAR4-Strep full length protein-synthetic nanodisc In Stock |
参考文献:
- Liu Y, Chen K, Wang C, et al. GPR84 regulates macrophage phagocytosis and innate immune responses. Nature Communications. 2023;14:41201.
- Wang J, Wu X, Simonavicius N, et al. GPR84 promotes NLRP3 inflammasome activation and inflammatory responses. Acta Pharmaceutica Sinica B. 2022;12(2):841-
- Zhang Q, Liu H, Chen J, et al. Targeting GPR84 reshapes tumor immune microenvironment and enhances immunotherapy. Cancer Immunology, Immunotherapy. 2023;72(11):3021-
- Schulze AS, Kleinau G, Krakowsky R, et al. Evolutionary analyses reveal immune cell receptor GPR84 as a conserved receptor for bacteria-derived molecules. iScience. 2022 Sep 6;25(10):105087.
- Audet M, Stevens RC. Emerging roles of GPR84 in inflammation and fibrosis: pharmacology and drug discovery. Frontiers in Pharmacology. 2024;15:1287654.
- Alvarez-Curto E, Milligan G. Metabolism meets immunity: the role of free fatty acid receptors such as GPR84. British Journal of Pharmacology. 2023;180(6):987-
- Nagy MA, et al. GPR84 links fatty acid sensing to immune and metabolic regulation. Journal of Clinical Investigation. 2023;133(12):e168992.
- Bouchard L, et al. GPR84 contributes to neutrophil recruitment and lung inflammation. American Journal of Respiratory Cell and Molecular Biology. 2023;69(4):456-
- Huang X, He S, Guo Y, et al. GPR84 as a potential therapeutic target in cancer and inflammation. Signal Transduction and Targeted Therapy. 2023;8:388.
- Li R, Zhao Y, Zhang M, et al. GPR84-mediated neuroinflammation and pyroptosis in CNS disorders. Journal of Neuroinflammation. 2024;21:112.


