2025年7月,Roche公布的trontinemab临床数据再次点燃了血脑屏障(BBB)递送领域的关注。trontinemab是一种工程化的双特异性抗体:一端结合致病靶点(如Aβ),另一端结合转铁蛋白受体1(TfR1)。通过TfR1,trontinemab能够从血液主动进入脑内,从而显著提升抗体的脑内暴露与作用效率。更新的临床数据显示,在3.6 mg/kg剂量下,约91%的患者在28周后实现淀粉样蛋白PET阴性,且ARIA-E发生率低于5%;同时,该分子已进入III期临床(TRONTIER 1/2),标志着TfR1介导的脑递送策略首次迈入大规模临床验证阶段。这也使TfR1从一个铁代谢相关蛋白,转变为当前最具转化价值的脑递送入口之一。
一、TfR1与转铁蛋白受体家族
转铁蛋白受体(transferrin receptor, TfR)家族主要包括转铁蛋白受体1(TfR1)和转铁蛋白受体2(TfR2)两种亚型。其中,TfR1是该家族中表达最广泛、功能研究最充分的一类成员,而TfR2则更多参与肝脏铁稳态与系统性铁代谢调控,在组织分布与生理功能上具有一定特异性。
TfR1,又称为CD71,由TFRC基因编码。人源TFRC基因定位于染色体3q29区,基因全长约30 kb,包含多个外显子与内含子结构。该基因编码的TfR1蛋白是一条包含760个氨基酸的多肽链,分子量约为85-95 kDa。TfR1是典型的Ⅱ型跨膜糖蛋白,包括一个N端胞内区、一个跨膜区和一个C端胞外区。其N端胞内区,位于细胞质侧,包含关键的内吞信号序列,负责介导受体的网格蛋白依赖性内吞,是启动铁摄取循环的功能核心之一。单次跨膜区将蛋白稳定锚定于细胞膜上,并维持其空间取向。蛋白的大部分区域为C端胞外结构域,该区域形成稳定的同源二聚体结构,并包含转铁蛋白结合位点,是实现配体识别与结合的关键功能区。结构研究表明,两条TfR1多肽链通过Cys89和Cys98形成的二硫键连接,维持二聚体稳定性,从而保障其高效的配体结合能力。此外,TfR1可在特定位点(如Arg100附近)发生蛋白水解,释放胞外结构域形成可溶性TfR1(sTfR)。这一跨膜型与可溶型并存的特性,使TfR1不仅是铁代谢的关键分子,也成为具有调控与检测价值的重要生物标志物[1][2]。
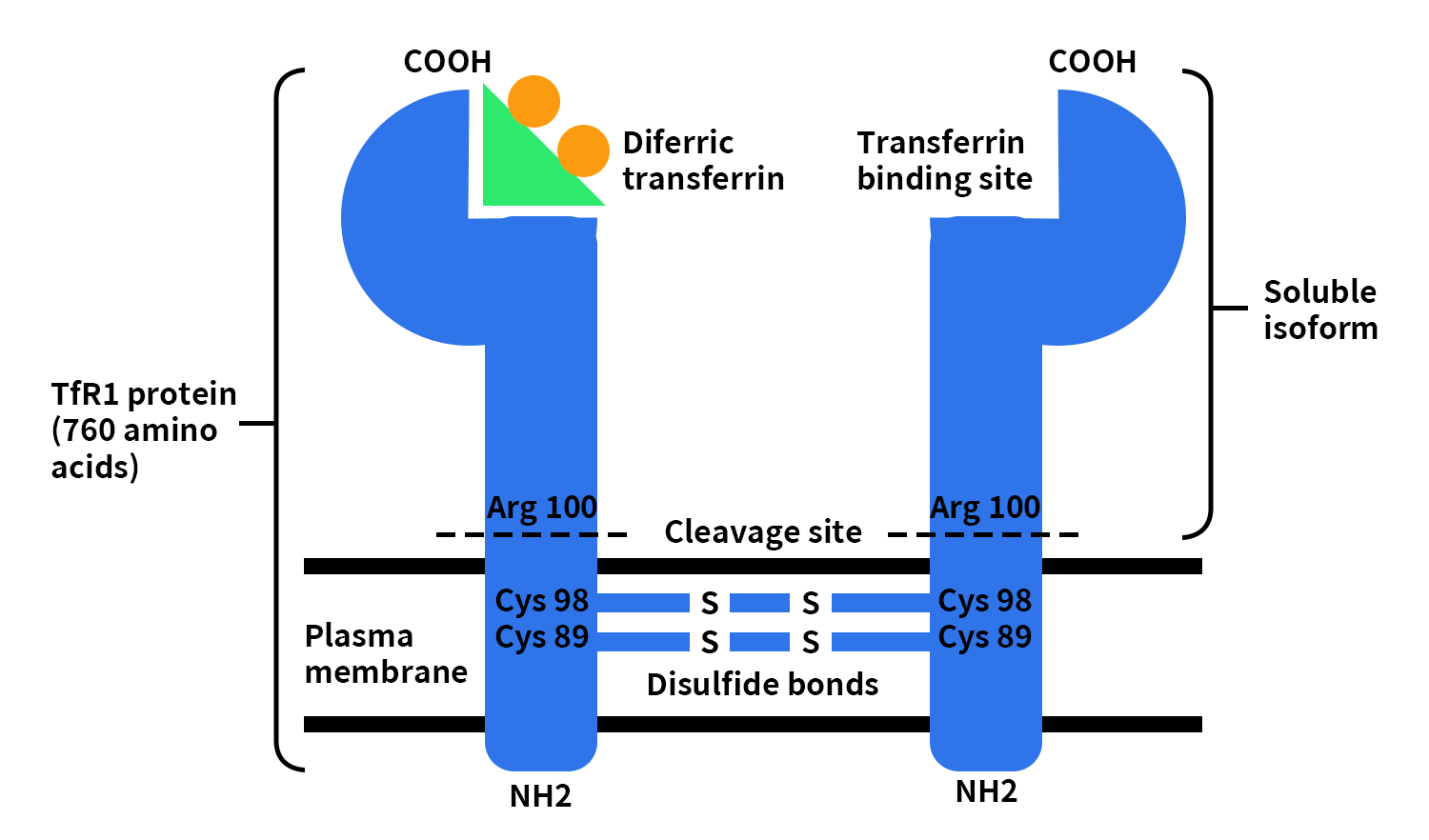
Figure 1. The picture of TfR1 structure [3]
二、TfR1的表达与生理功能
TfR1广泛表达于多种细胞类型,尤其在铁需求较高的组织或细胞中表达更为显著,包括红系前体细胞、肿瘤细胞以及脑微血管内皮细胞[2]。TfR1的核心作用是维持细胞内铁稳态。通过与转铁蛋白结合并介导内吞,TfR1将铁输送入细胞,用于DNA合成、线粒体代谢等关键过程[2,4]。此外,TfR1还具有高频循环特性,即在完成一次内吞过程后可以迅速回到细胞表面继续参与运输,这一“高通量循环系统”使其在药物递送中具备独特优势。
三、TfR1在BBB中的调控机制
在血脑屏障中,TfR1高表达于脑微血管内皮细胞的血管腔侧。它不仅是铁代谢的核心分子,同时也承担着分子跨胞转运的重要功能,是血液中分子进入脑内的重要入口之一[5]。如下图所示,生理条件下,TfR1首先与携带三价铁(Fe3+)的转铁蛋白结合,并通过受体介导内吞进入脑微血管内皮细胞。在内体酸性环境中,Fe3+被还原为Fe2+并释放,经由二价金属转运蛋白1(DMT1)转运进入细胞质,随后通过ferroportin输出至脑侧,再被氧化为Fe3+重新加载至脑间质转铁蛋白,从而完成跨BBB的铁供应过程。与此同时,去铁转铁蛋白仍与TfR1结合并循环回细胞表面,在中性环境中解离,使受体得以重复利用。
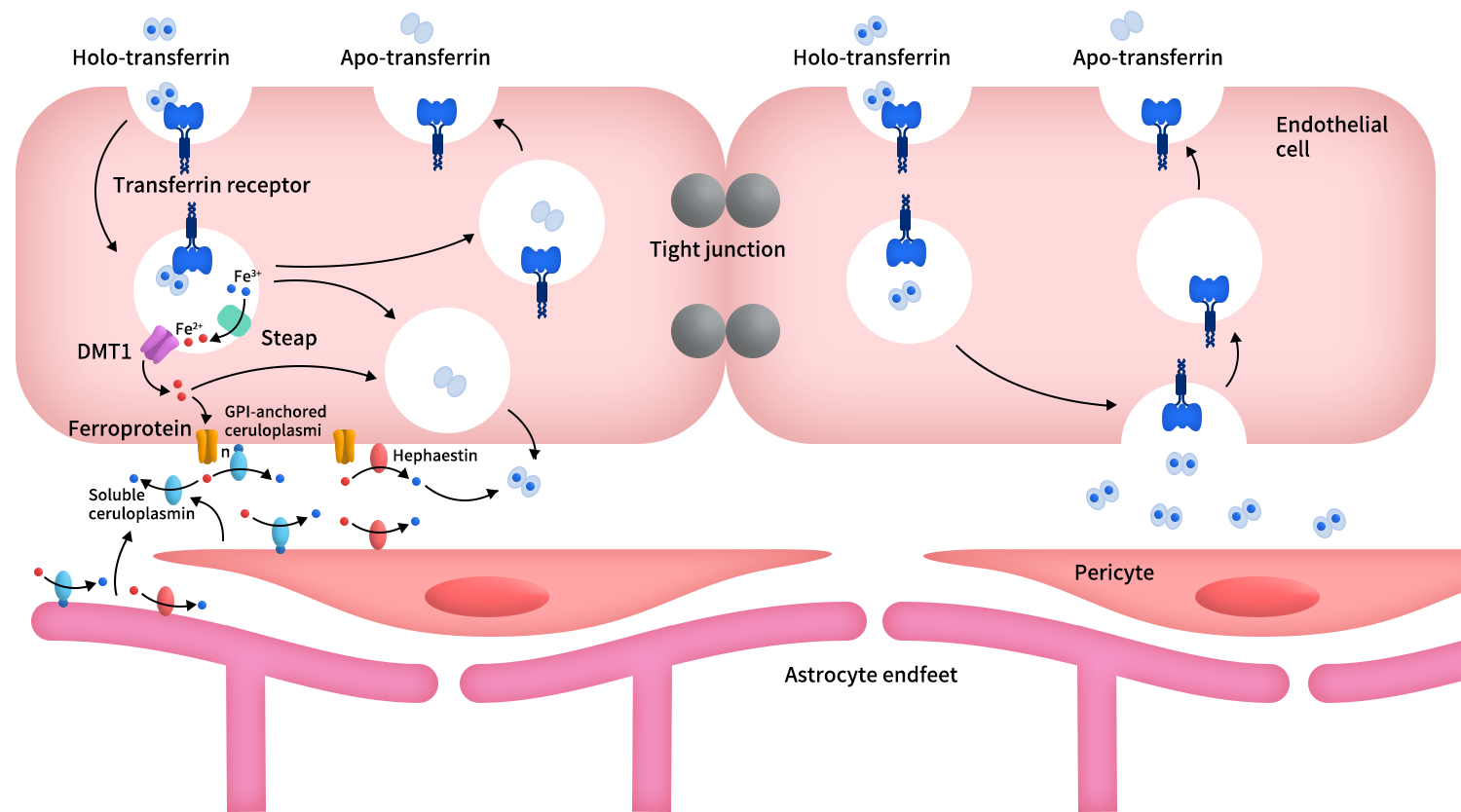
除了这一经典的铁转运路径外,TfR1还具备受体介导跨胞转运能力。部分与TfR1结合的配体(如工程化抗体)在内吞后并不发生降解或释放,而是通过囊泡运输跨越内皮细胞,在脑侧整体释放。这一跨胞转运路径避免了分子在细胞内的分解,使TfR1成为当前大分子药物进入脑内最重要的天然入口之一[4,5]。
但这一过程并非简单的结合即转运。研究表明,TfR1介导的跨胞效率高度依赖抗体或配体的设计方式。例如,过高的结合亲和力可能导致复合物进入溶酶体降解,而适中的亲和力更有利于跨胞转运[7]。同时,结合价态和表位选择也会显著影响受体的内吞路径及最终命运[5,7]。
四、TfR1靶向药物的临床研究进展
近年来,TfR1相关策略已从理论研究逐步进入临床验证阶段。不完全统计,全球靶向TfR1的药物管线共计114条,其中30条处于药物发现,58条处于临床前阶段,已上市的只有1款,处于临床阶段的11款。尽管上市及临床阶段的药物数量并不多,但药物类型丰富,包括双特异性抗体、抗体核酸偶联药物(AOC)、单克隆抗体及抗体偶联药物(ADC)等。关于涉及领域,目前,TfR1策略正被拓展至多个方向,包括阿尔茨海默病、帕金森病、脑肿瘤以及核酸药物递送等[5,8]。
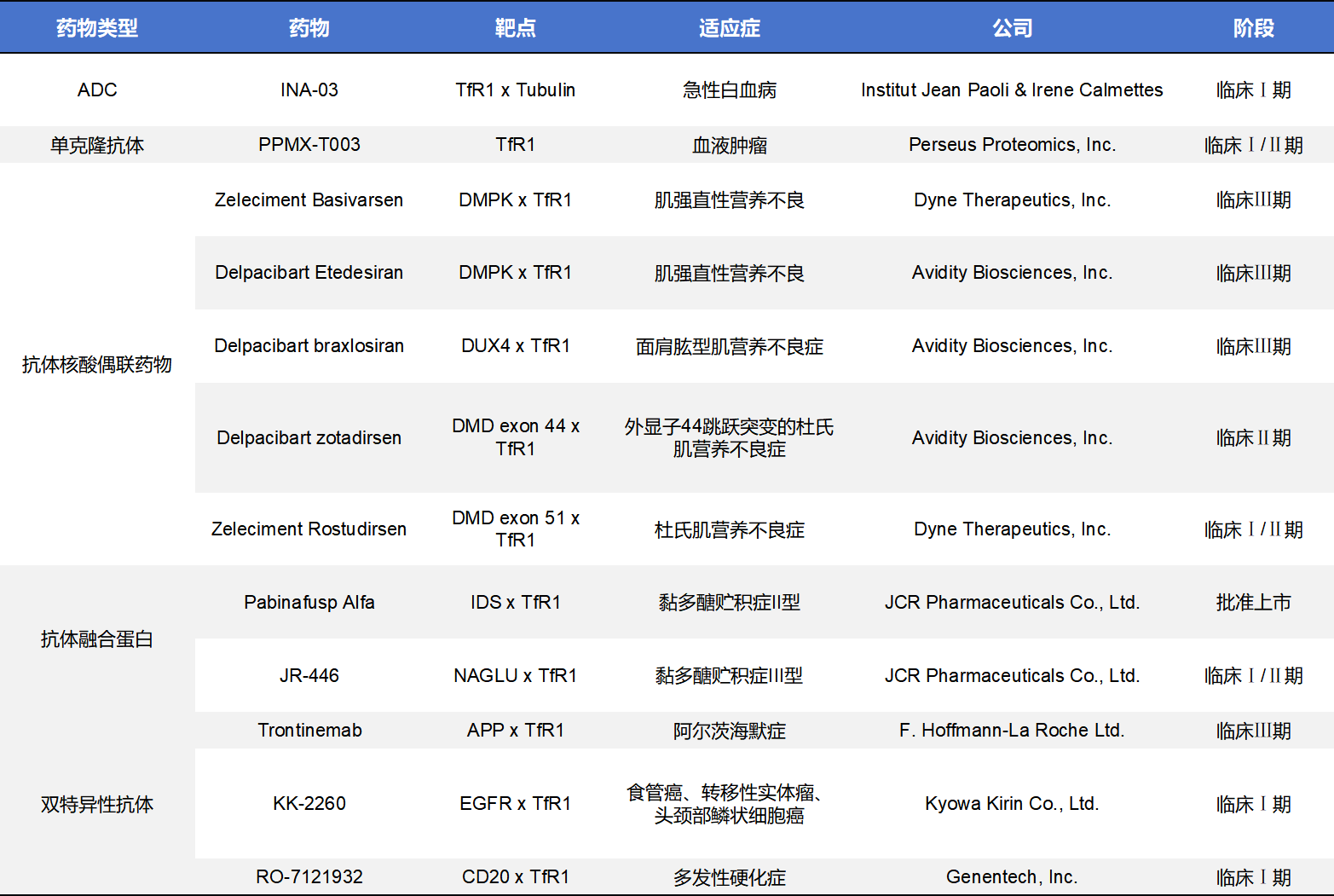
4.1 TfR1 ADC
目前已进入临床阶段靶向TfR1的ADC药物仅一款,NA-03。该药是由Institut Paoli-Calmettes(IPC)联合Inatherys开发的一款靶向TfR1的ADC药物,目前处于Phase I临床研究阶段(NCT03957915),主要用于复发/难治性急性髓系白血病(AML)及急性淋巴细胞白血病(ALL)。其作用机制基于TfR1在高增殖肿瘤细胞中的高表达特征:抗体部分特异性结合TfR1并竞争性干扰转铁蛋白介导的铁摄取,同时促进受体复合物内吞进入溶酶体,释放微管抑制剂MMAE,从而诱导细胞周期阻滞与肿瘤细胞凋亡。早期临床数据显示其在部分患者中可观察到骨髓原始细胞下降及一定缓解信号,但由于CD71在正常造血系统亦有表达,治疗相关骨髓抑制为主要剂量限制毒性。
4.2 TfR1单克隆抗体
PPMX-T003是由Perseus Proteomics, Inc.开发的一款靶向TfR1的人源单抗,属于一类以“铁代谢通路”为基础的新型抗体治疗药物。其作用机制是通过结合TfR1,抑制肿瘤或异常增殖细胞的铁摄取,从而干扰红系前体细胞及肿瘤细胞的增殖,同时通过降低铁利用效率实现抗肿瘤细胞增生效应,并不依赖传统细胞毒性通路。该药最早用于真性红细胞增多症(PV),并延伸至急性NK细胞白血病(ANKL)等血液肿瘤适应症。目前PPMX-T003已完成PV相关的Phase I试验,结果显示可降低红细胞参数并在部分患者中实现减少或避免放血治疗,同时安全性总体可控;针对ANKL的研究者发起I/II期试验仍在进行中,但由于该疾病极其罕见,入组进展较慢并已延长研究周期。
4.3 靶向TfR1的AOC
AOC是一类将抗体与寡核苷酸(如siRNA、ASO)通过化学或连接子偶联的药物形式。其核心是利用抗体识别特定受体(如TfR1)实现组织或细胞特异性递送,再由核酸分子在细胞内发挥基因调控作用(如沉默、剪接调控)。在肌肉疾病领域,TfR1因在肌细胞中表达较高,被广泛用于提升核酸药物的摄取效率。针对TfR1靶点,布局了该靶点且管线已进入临床的玩家以Dyne Therapeutics和Avidity Biosciences为代表。二者均围绕TfR1构建差异化递送平台,推动核酸药物在肌病领域的转化,是该领域的直接竞争对手。
- Dyne Therapeutics(Zeleciment Basivarsen & Zeleciment Rostudirsen)
目前Dyne Therapeutics拥有的两款TfR1相关的AOC药物,分别是Zeleciment Basivarsen和Zeleciment Rostudirsen。其中,Zeleciment Basivarsen通过将靶向DMPK的寡核苷酸与TfR1结合抗体偶联,借助TfR1介导的内吞作用实现肌细胞递送,用于治疗肌强直性营养不良(DM1)。其机制在于降低致病性DMPK转录本,从而缓解毒性RNA效应。目前已进入III期临床,显示出较好的靶向递送能力。而Zeleciment Rostudirsen是针对DMD exon 51突变,也是采用TfR1抗体偶联ASO策略,提高核酸在肌肉中的分布与摄取。其机制同样基于外显子跳跃,恢复dystrophin蛋白表达。目前处于I/II期临床阶段。
- Avidity Biosciences(Delpacibart Etedesiran & Delpacibart braxlosiran & Delpacibart zotadirsen)
在围绕TfR1构建差异化递送平台这块,Avidity Biosciences目前进入临床阶段的管线有三条,分别是Delpacibart Etedesiran、Delpacibart braxlosiran和Delpacibart zotadirsen。Delpacibart Etedesiran靶向DMPK,通过TfR1介导进入肌细胞后释放siRNA,降低异常RNA表达。是Avidity AOC平台的代表项目之一,目前已进入III期临床,显示出良好的分子下调效率和安全性。
- Delpacibart braxlosiran针对DUX4基因,用于面肩肱型肌营养不良症(FSHD)。通过TfR1靶向递送siRNA至肌肉组织,抑制DUX4表达,从源头干预疾病进展。目前也处于III期临床阶段,是FSHD领域较受关注的核酸疗法之一。该项目进一步验证了TfR1在骨骼肌递送中的通用性。
- Delpacibart zotadirsen靶向DMD基因exon 44突变,通过TfR1递送反义寡核苷酸(ASO),促进外显子跳跃,从而恢复部分功能性蛋白表达。当前处于II期临床阶段。相比传统ASO,TfR1介导递送有望显著提升肌肉摄取效率,是杜氏肌营养不良症(DMD)治疗的重要优化方向。
4.4 TfR1抗体融合蛋白
抗体融合蛋白是将功能性蛋白(如酶、配体)与抗体或其片段进行基因融合形成的重组分子。其核心优势在于:利用抗体的靶向能力(如结合TfR1)实现特定组织递送,同时由融合的功能蛋白在靶组织内发挥治疗作用。在中枢神经系统疾病中,这类分子常借助TfR1实现跨BBB递送。
- Pabinafusp Alfa是由JCR Pharmaceuticals开发的一种将艾杜糖-2-硫酸酯酶(IDS)与抗TfR1抗体融合的重组蛋白,用于治疗II型黏多糖贮积症(MPS II)。其通过TfR1介导跨BBB转运,将酶递送至中枢神经系统,从而降解异常积累的糖胺聚糖。该药已在日本获批上市,是首个验证TfR1脑递送策略商业化可行性的产品[8]。
- JR-446也是由JCR Pharmaceuticals开发,是一款NAGLU酶与TfR1抗体融合的候选药物,针对III型黏多糖贮积症(MPS III)。其设计逻辑与Pabinafusp Alfa类似,通过TfR1介导进入脑内,补充缺失酶以清除底物积累。目前处于I/II期临床阶段。该项目延续了 JCR Pharmaceuticals 在TfR1递送平台上的开发路径,进一步拓展其在溶酶体贮积病领域的应用潜力。
4.5 双特异性抗体
双特异性抗体是一类可同时识别两个不同靶点的工程化抗体。即一端结合治疗靶点,另一端结合递送或功能相关靶点(如TfR1),从而实现靶向作用与定向递送的双重功能。在中枢神经系统和肿瘤领域,TfR1常被用作入口靶点,帮助抗体跨血脑屏障或提升组织分布。
- Trontinemab是一款由Roche开发,基于其Brainshuttle™平台推进的双特异性抗体。通过同时结合Aβ与TfR1,实现脑内靶点作用与跨BBB递送的协同。其利用TfR1介导的跨胞转运进入脑组织,提高抗体在中枢的暴露水平,用于治疗阿尔茨海默症。目前已进入III期临床(TRONTIER 1/2),是TfR1脑递送策略最具代表性的临床项目之一[9][10]。
- KK-2260,由Kyowa Kirin开发,是一款靶向EGFR与TfR1的双特异性抗体,主要用于食管癌、头颈部鳞癌及转移性实体瘤。其设计思路是在肿瘤治疗中引入TfR1,以增强抗体在肿瘤组织中的分布或潜在跨屏障能力,同时发挥EGFR抑制作用。目前处于I期临床阶段。
- RO-7121932,由Genentech, Inc.开发,可同时结合CD20与TfR1,旨在将B细胞清除作用拓展至中枢神经系统,用于多发性硬化症治疗。通过TfR1介导的BBB转运,该分子有望提升抗CD20疗法在脑内的有效性。目前处于I期临床阶段,是抗体跨BBB治疗神经免疫疾病的重要探索方向。
五、缔码生物的TfR1相关产品
随着TfR1在脑递送领域的重要性不断提升,高质量的实验工具成为推动项目进展的重要基础。缔码生物围绕TfR1/TFRC提供了覆盖重组蛋白、抗体、稳转细胞株及Biosimilar阳参抗体等多类型工具产品,可满足从靶点验证到功能研究的完整需求。
其中,缔码生物提供的TfR1重组蛋白采用HEK293表达,以胞外结构域(ECD)为核心,并结合His、Fc等标签或多价形式构建。ECD可保留天然结合位点,适用于抗体筛选及亲和力检测(ELISA/BLI/SPR);Fc融合或多聚化设计则提升稳定性,更贴近天然受体状态,利于功能筛选与机制研究。同时,产品覆盖人、小鼠及食蟹猴等物种,支持跨物种研究,尤其适用于抗体开发及BBB穿梭项目中的交叉反应性评估。
此外,公司还提供TfR1相关biosimilar参考抗体、流式及标记抗体,以及稳转细胞株,支持FACS分析与功能验证。整体产品体系可广泛应用于抗体发现与机制研究,并拓展至CD98hc、GLUT1、IGF-1R等BBB靶点,助力脑递送药物开发。
除了蛋白抗体,缔码生物作为一家专注于可成药靶点临床前研发产品和服务的生物技术公司。依托其自主创新单B细胞抗体发现平台、抗体工程改造平台及功能验证平台已成功筛选出多个BBB相关的功能性抗体分子,更多功能数据,欢迎留言垂询。

参考文献
- Kawabata H. Transferrin and transferrin receptors update. Free Radical Biology and Medicine, 2019.
- Gammella E, et al. Iron metabolism in health and disease. International Journal of Molecular Sciences, 2017.
- Harms, Kristian and Thorsten Kaiser. Beyond soluble transferrin receptor: old challenges and new horizons. Best practice & research. Clinical endocrinology & metabolism 29 5 (2015): 799-810.
- Torti SV, Torti FM. Iron and cancer: more ore to be mined. Nature Reviews Cancer, 2013.
- Daneman R, Prat A. The blood–brain barrier. Cold Spring Harbor Perspectives in Biology, 2015.
- Shen, X.; Li, H.; Zhang, B.; Li, Y.; Zhu, Z. Targeting Transferrin Receptor 1 for Enhancing Drug Delivery Through the Blood–Brain Barrier for Alzheimer’s Disease. Int. J. Mol. Sci. 2025, 26, 9793.
- Pardridge WM. Blood–brain barrier and delivery of protein therapeutics. NeuroRx, 2020.
- Bien-Ly N, et al. Transferrin receptor-mediated transcytosis of antibodies. Journal of Experimental Medicine, 2014.
- Sonoda H, et al. A blood-brain-barrier-penetrating antibody–enzyme fusion protein. Nature Biotechnology, 2018.
- Roche clinical updates on trontinemab, 2025.


