在2025年美国临床肿瘤学会(ASCO)年会上,靶向CCR8的创新管线再次惊艳亮相。例如,礼新医药与中国生物制药联合开发的LM-108,在针对既往一线治疗失败的晚期胰腺癌及胃癌的临床研究中,展示了显著的疗效,尤其是在CCR8高表达亚组中,客观缓解率(ORR)远超现有的标准治疗。与此同时,诺诚健华的ICP-B05在皮肤T细胞淋巴瘤(CTCL)中也展现了“定点爆破”肿瘤Treg的能力,6个月无进展生存率(PFS)达72.9%。
这种爆发性的临床表现直接点燃了BD交易市场,各大跨国药企纷纷重金押注。从百时美施贵宝(BMS)以高达15.6亿美元的里程碑付款金额与Agenus达成合作,到吉利德(Gilead)斥资6.7亿美元(包括1亿美元首付款)收购Jounce的CCR8抗体项目,这一赛道的火热程度不言而喻。巨头们之所以如此青睐这一靶点,核心在于CCR8在肿瘤浸润Treg(TITRs)上具有极度特异性的高表达,这使得药物能够精准“定位”并清除肿瘤内部的免疫抑制细胞,而不会像传统靶点那样引起全身性的免疫副作用。CCR8已成为抗PD-1/L1耐药后的关键补位选手,更是开启肿瘤精准免疫2.0时代的关键钥匙。
1、CCR8的结构与分布
趋化因子受体8(Chemokine receptor 8,CCR8)属于A类G蛋白偶联受体(GPCR)成员,属于趋化因子受体C-C亚家族。CCR8蛋CCR8蛋白由355个氨基酸组成,具有典型的七次跨膜螺旋(7TM)结构。其N端暴露于胞外,负责识别趋化因子配体;C端位于胞内,与G蛋白结合触发信号转导。
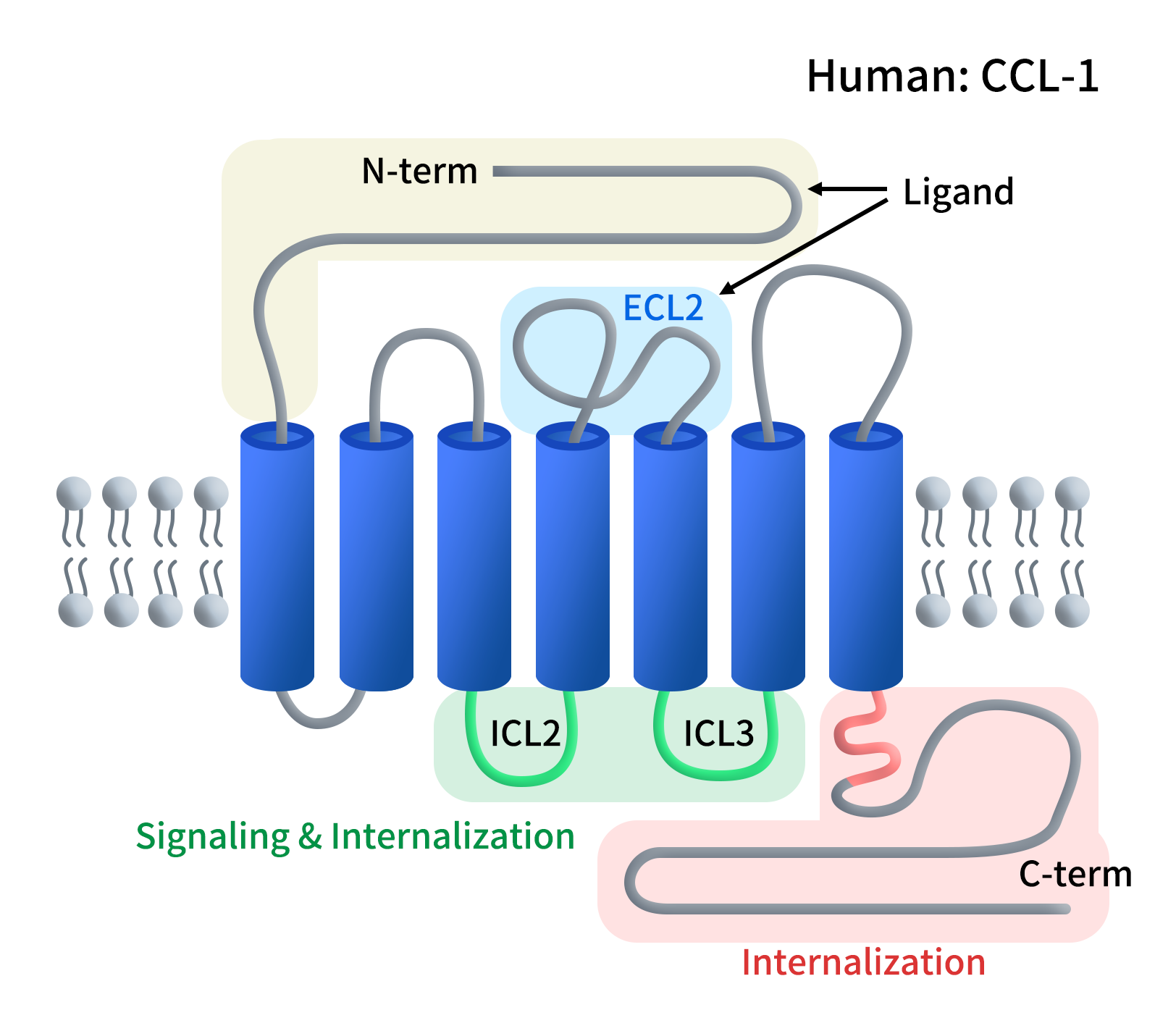
Figure 1. The structure of CCR8
CCR8的分布极度差异化。CCR8在Th2细胞、单核细胞和NK细胞上有表达,在Th1细胞上不表达。重点来了,CCR8在外周血、正常淋巴结或健康组织中的Treg上表达极低,但在肿瘤浸润调节性T细胞(TITRs)上呈现特异性极高的表达,特别是在乳腺癌、肺癌、结直肠癌和胃癌等实体瘤中。
2、CCR8功能与相关疾病
在生理状态下,CCR8参与Th2细胞的募集和皮肤、粘膜的免疫稳态;在病理状态下,CCR8通过与其配体CCL1相互作用招募FOXp3+、CCR8+Treg细胞浸润到肿瘤组织中,行使免疫抑制功能,同时可以诱导FOXp3+Treg细胞表面CCR8表达上调,诱发Ca2+流动,诱导stat3依赖性的Foxp3、CD39、IL-10和颗粒酶B表达上调,进而增强这些肿瘤浸润的Treg细胞的免疫抑制活性,从而形成强大的免疫抑制屏障,阻断杀伤性T细胞(CD8+ T)的进入。
结合CCR8的功能,目前与CCR8相关的疾病主要包括肿瘤与自身免疫疾病,其中恶性肿瘤依然是CCR8当前的主战场。通过耗竭CCR8+ Treg,可以解除TME的抑制,与PD-1单抗产生协同效应。在自身免疫性疾病,尤其是特应性皮炎(AD)和哮喘中,CCR8介导了Th2细胞的异常聚集。开发CCR8拮抗剂或激动剂(用于增强Treg抑制)是治疗过敏性炎症的新方向。此外,部分研究指出CCR8在某些组织纤维化过程中参与了巨噬细胞的招募。
3、CCR8与其配体在肿瘤中的作用
人类CCR8有四种已知配体:CCL1、CCL8、CCL16和CCL18。其中,最主要的是CCL1。人CCL1可同时与CCR8细胞外环2 (ECL2)和CCR8的N端结构域结合。尽管CCR8也能与CCL8、CCL16及某些病毒趋化因子结合,但CCL1-CCR8轴是驱动Treg迁移和功能的绝对核心。
3.1 CCL1-CCR8轴在肿瘤中的作用
CCR8在肿瘤浸润的Treg细胞中高表达,而CCL1主要由肿瘤相关成纤维细胞(CAF)、肿瘤相关巨噬细胞(TAM)、肿瘤浸润Treg以及部分肿瘤干细胞产生。在肿瘤微环境中,CCL1激活癌细胞上的CCR8受体,导致癌细胞的增殖、凋亡抗性和迁移。除了对癌细胞的作用外,CCL1通过激活内皮细胞上的CCR8受体引起血管生成。CCL1另一个重要功能是募集Treg到肿瘤生态位,并参与了CD4+ T细胞向Treg的转化。CD4+ T细胞向Treg的转化过程依赖于转化生长因子-β ( TGF-β)。CCL1支持Treg在肿瘤生态位中的免疫抑制功能。阻断CCL1-CCR8轴作为一种新的基于免疫检查点的恶性肿瘤治疗方法。
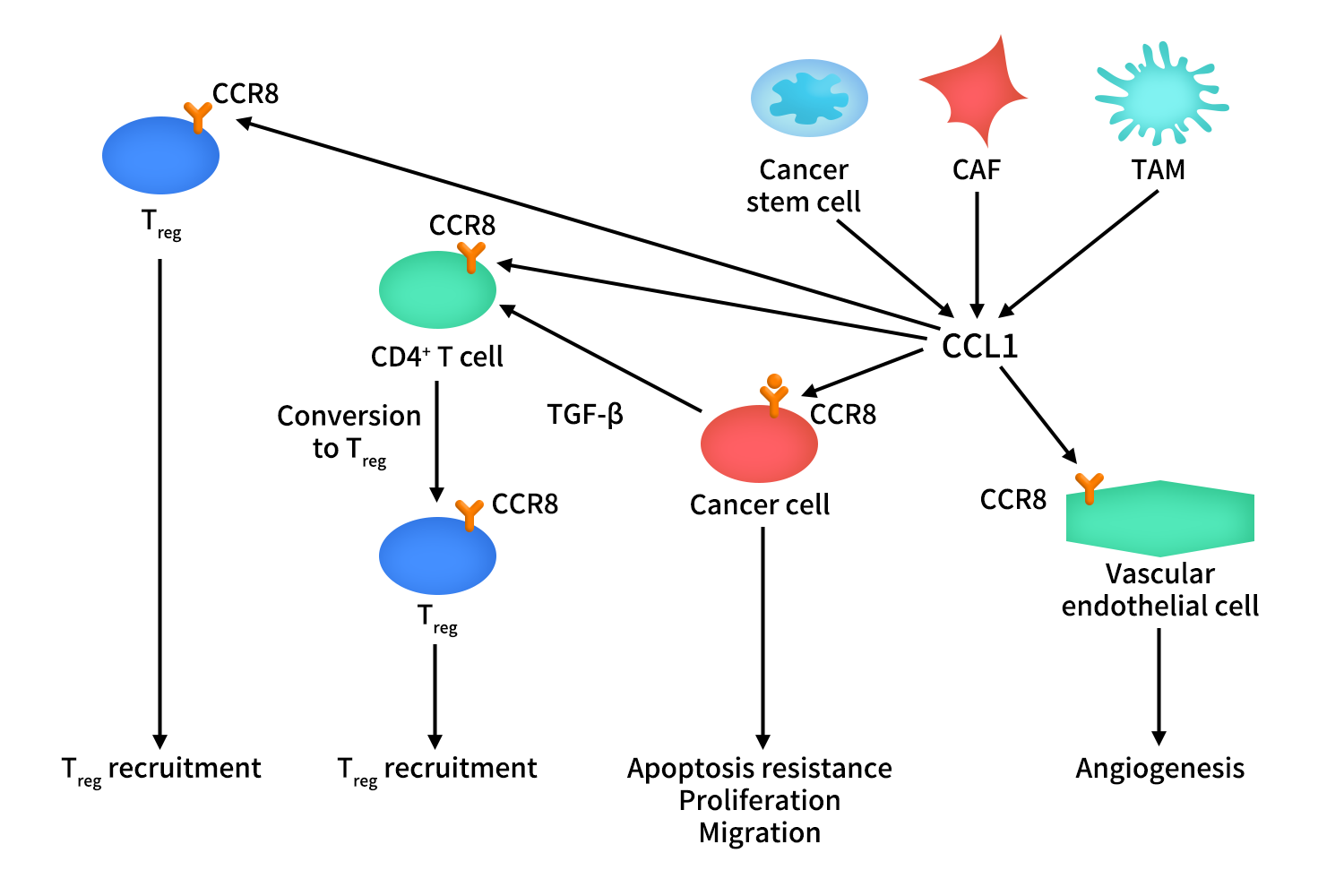
Figure 2. The mechanism of CCR8-CCL1 axis in cancer [1]
3.2 CCL18-CCR8在癌症中的作用
在肿瘤中,CCL18由TAM产生和分泌,它以自分泌的方式作用于这些细胞。它还通过受体PITPNM3和CCR8引起癌细胞迁移和侵袭。CCL18通过作用于内皮细胞上的PITPNM3而在血管生成中起重要作用。它还导致naïve CD4+ T细胞进入肿瘤生态位和 CD4+ T细胞向Treg细胞的转化。
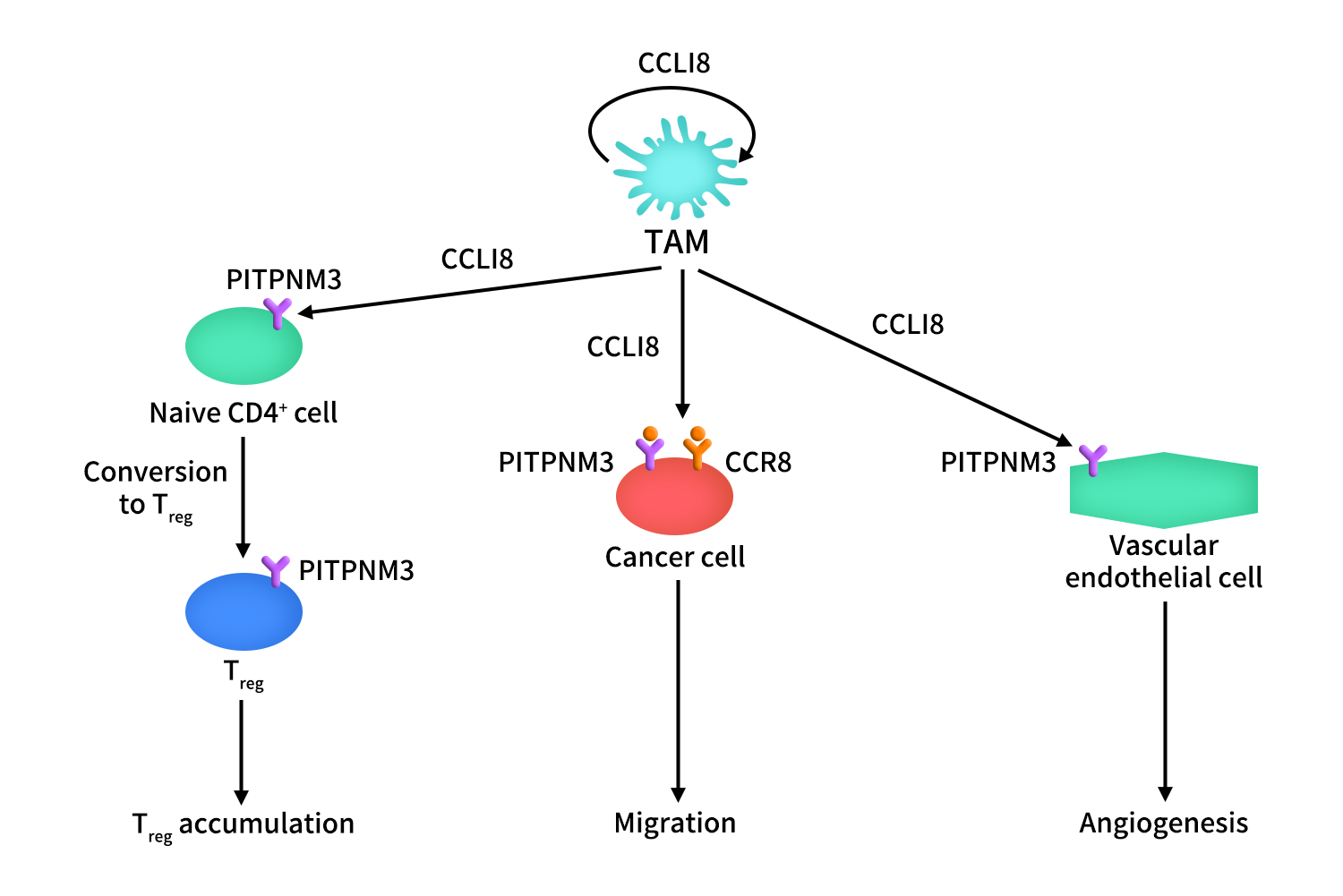
Figure 3. The mechanism of CCR8-CCL18 axis in cancer [1]
4、靶向CCR8疗法临床研究进展
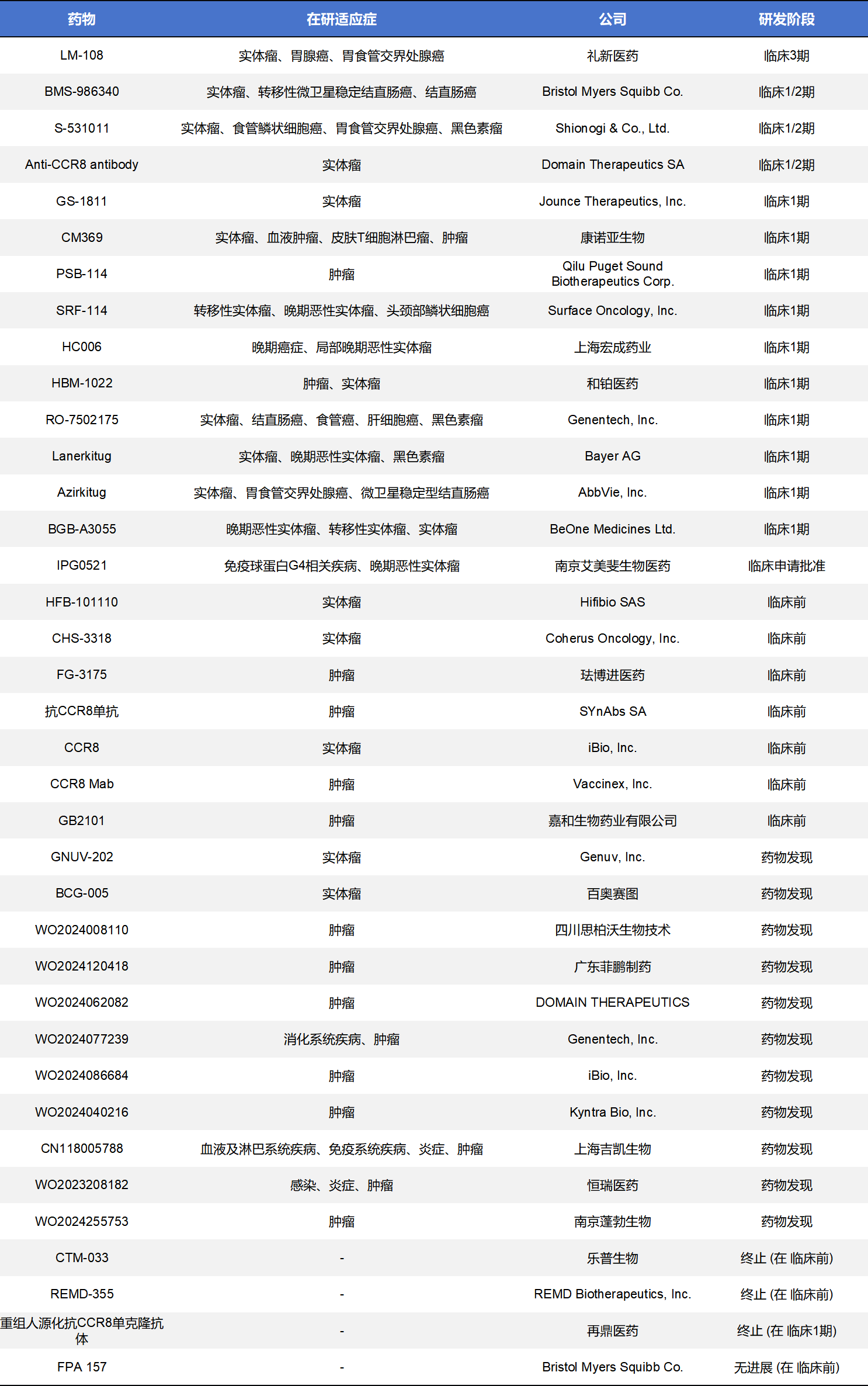
肿瘤部位的Treg上的CCR8特异性高表达表明CCR8是肿瘤部位的Treg细胞的非常好的生物标志物,是极具潜力的肿瘤免疫靶点,也是目前CCR8药物开发的主战场。不完全统计,目前全球CCR8药物共计有73款,其中临床前阶段有23款,药物发现阶段的有16款,处于临床1期的有11款,临床2期和3期的仅4款。其药物类型主要集中在单克隆抗体和小分子拮抗剂。不过其他类型药物,比如双特异性抗体、ADC药物、CAR-T也有少量管线。这里重点展示了单克隆抗体级小分子化药。
4.1 CCR8单克隆抗体
这类CCR8药物目前进出临床阶段的共有14款,其中处于临床3期只有一款,多数还是处于临床1期。
- LM-108,商品名为Cafelkibart,由礼新医药主导研发的一种靶向CCR8的人源化抗体,通过 抗体依赖性细胞介导的细胞毒(ADCC)和抗体依赖性细胞吞噬(ADCP)作用选择性清除肿瘤微环境中表达CCR8的调节性T细胞(Tregs),缓解免疫抑制并增强肿瘤免疫反应。2025 ASCO数据显示,其联合PD-1在晚期胰腺癌中观察到3%的ORR,这在“癌中之王”中已是重大突破。目前,LM-108已启动III期注册临床试验(NCT07362186),作为二线治疗(联合 toripalimab 对比紫杉醇)用于 CCR8 阳性局部晚期或转移性胃癌/胃食管结合部腺癌患者,该试验计划在中国展开并进入随机对照阶段,是迄今为止该药进入的最高阶段试验。
- BMS-986340,商品名为Imzokitug,是一种非岩藻糖化(afucosylated)人源化CCR8 IgG1抗体。非岩藻糖化设计增强了Fc与效应细胞的结合,从而增强ADCC活性,更有效地清除肿瘤浸润的CCR8-阳性调节性T细胞,旨在改善肿瘤免疫微环境并激活抗肿瘤免疫。BMS-986340正在进行全球I/II期试验,包括单药治疗及与PD-1抑制剂联合治疗的研究,以评估其安全性、耐受性和初步疗效,目前处于招募与剂量递增阶段。尚无公开发表的对比性临床结果报告,但多个试验活跃进行中,覆盖多种实体瘤类型,包括胰腺癌及微卫星稳定性(MSS)结直肠癌等。
- S-531011是一款由Shionogi开发的人源化IgG1单克隆抗体,特异性识别CCR8,具有强大的ADCC和阻断CCR8-CCL1信号的能力,从而削弱CCR8+调节性T细胞在肿瘤微环境中的免疫抑制功能,恢复和增强抗肿瘤免疫。该药物目前已在临床前模型中显示出减少肿瘤浸润性Tregs并显著抑制肿瘤生长的能力,且在小鼠模型中与PD-1抑制剂联合治疗显示更强的抗肿瘤效应,且尚未观察严重不良反应。当前S-531011正在日本和美国推进 Phase 1b/2 试验,以评估其安全性、推荐剂量和初步疗效。
- GS-1811,商品名为Denikitug,由Jounce Therapeutics开发,是一种靶向CCR8的非岩藻糖化人源化单克隆抗体,设计用于选择性清除肿瘤微环境中高表达CCR8的免疫抑制性肿瘤浸润调节性T细胞(Tregs)。通过增强的ADCC作用,阻断CCR8-CCL1信号并诱导CCR8+ Tregs细胞死亡,从而试图解除免疫抑制、激活抗肿瘤免疫反应。目前,该药正在开展一项I期(首人人体)临床试验(NCT05007782),评估单药及与抗PD-1抗体zimberelimab联合用药在晚期实体瘤患者中的安全性、耐受性、最大耐受剂量和推荐II期剂量,试验仍处于招募/开展状态。吉利德于2022年收购了该候选药的全部剩余开发权。
4.2. CCR8小分子拮抗剂
这类CCR8药物目前进出临床阶段的共有7款,仅一款进入临床。即由艾美斐开发的IPG-7236。该药作为口服小分子拮抗剂,通过阻断CCL1/CCR8轴干扰Treg的募集,具有更好的组织渗透性和给药便利性。目前IPG-7236已进入临床I/II 期人体研究。当前正在开展一项多中心、开放标签的剂量递增及扩展研究,旨在评估该药在 晚期实体瘤患者中的安全性、耐受性、药代动力学和初步抗肿瘤活性,并涵盖包括肾癌、三阴性乳腺癌、头颈部肿瘤和黑色素瘤等实体瘤亚型。此外,艾美斐已与上海GoBroad癌症医院建立战略合作,加速IPG-7236从I期向II期过渡开发,进一步推进其临床验证。
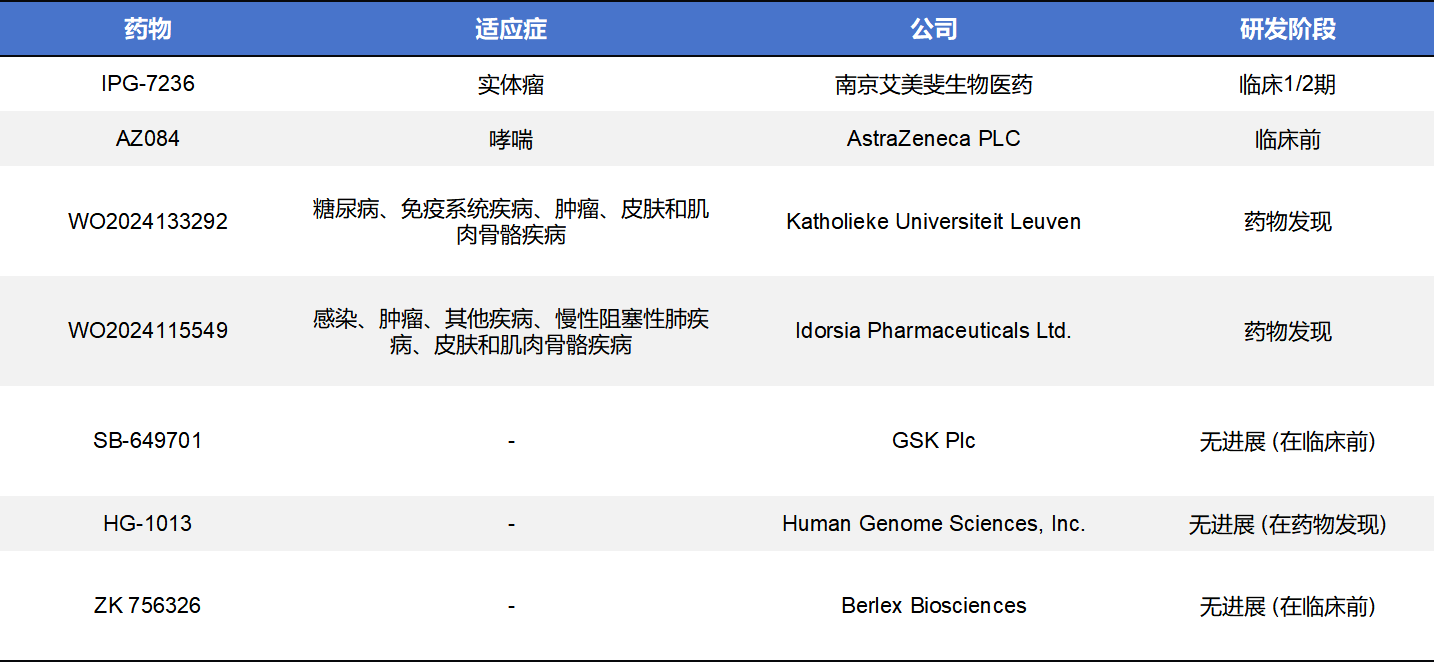
4.3其他类型CCR8药物
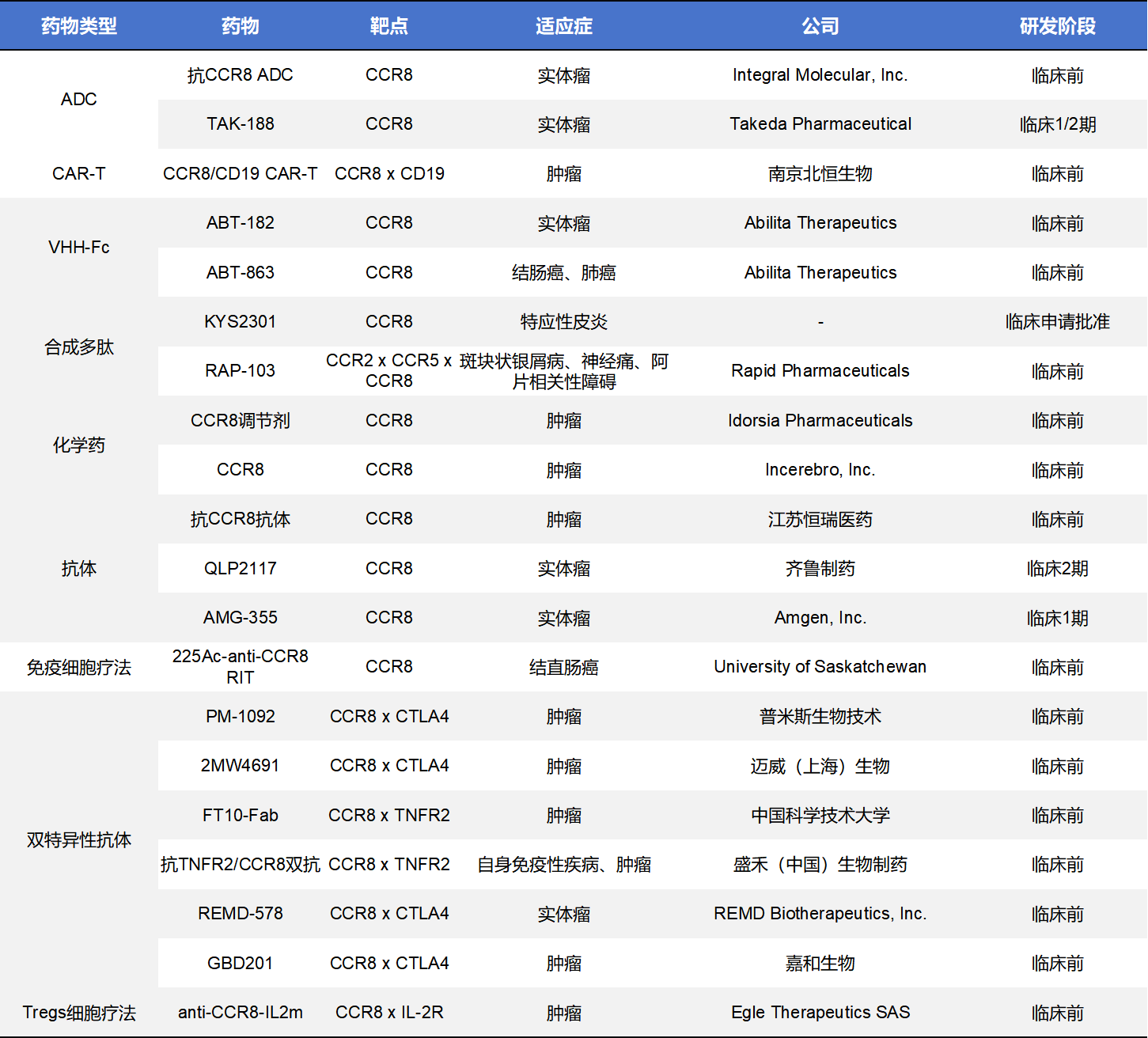
除了单克隆抗体和小分子药物,靶向CCR8的药物类型还包括ADC、CAR-T、化学药、双特异性抗体等,其中数量最多的是双特异性抗体,但均在临床前阶段。这些药物中,进入临床阶段的有3款,分别是Takeda的TAK-188、齐鲁制药的QLP2117和Amgen的AMG-355。
- TAK-188是Takeda开发的一种靶向CCR8的ADC药物。该药物与CCR8结合后将细胞毒载荷直接递送至CCR8+细胞,从而清除这些抑制性细胞,改善抗肿瘤免疫反应。CCR8+ Tregs的减少有望增强CD8+ T细胞对肿瘤的攻击。TAK-188 当前正处于I/II 期剂量递增与扩展研究,适应症为既往标准治疗失败的局部晚期或转移性实体瘤,在包括头颈部鳞状细胞癌和非小细胞肺癌等多个队列中评估安全性、耐受性及初步疗效。该试验实际启动于2025年11月19日,预计在未来几年完成剂量确定与扩展队列入组。
- QLP2117是齐鲁制药开发的一种靶向CCR8的IgG1单克隆抗体,通过ADCC清除肿瘤微环境中CCR8+调节性T细胞(Tregs),解除免疫抑制,促进抗肿瘤免疫应答。该候选药物目前正进行I/II期临床试验,分别为单药Phase 1安全性研究以及与QL2107联合的Ib/II 期剂量扩展研究,目标是评估安全性、耐受性、药代动力学及初步疗效,适应症为晚期实体瘤。
- AMG-355 是Amgen开发的一种靶向CCR8的抗体,主要作用在肿瘤微环境中结合 CCR8受体,阻断CCR8-CCL1信号并清除CCR8+调节性T细胞,从而增强抗肿瘤免疫。CCR8主要在肿瘤浸润Tregs上高表达,与免疫抑制密切相关。 AMG-355目前处于I期首人人体研究阶段,这项临床试验正在评估其单药及与pembrolizumab(PD-1抑制剂)联合用药在晚期实体瘤(如结直肠癌、肺癌、胃癌等)患者中的安全性、耐受性及推荐 II 期剂量。
5、缔码生物CCR8相关产品助力CCR8生物药开发
缔码生物科技有限公司是一家专注于可成药靶点临床前研发产品和服务的生物技术公司。缔码现可提供CCR8靶点全系列产品与服务。产品包括活性蛋白、参照抗体和流式验证单克隆抗体;服务涵盖多种属蛋白抗体定制服务、抗体人源化和亲和力成熟服务。此外,为加速CCR8生物疗法的开发,缔码还制备了CCR8靶点单B细胞种子库,最快20天可获得先导抗体分子;同时,我们目前已筛选出多个CCR8先导分子,客户第二天可以拿到分子进行功能评估验证;针对部分分子,我们也正在进行ADC内吞活性及杀伤验证,具体数据欢迎垂询。
| 产品类型 | 产品货号 | 产品名称 |
| ECD重组蛋白 | PME101103 | Human CCR8 Protein, mFc Tag |
| PME101091 | Human CCR8 Protein, hFc Tag | |
| PME-C100006 | Cynomolgus CCR8 Protein, hFc Tag | |
| PME-M100034 | Mouse CCR8 Protein, hFc Tag | |
| 全长蛋白 | FLP100001 | Human CCR8 full-length protein-MNP |
| FLP100037 | Human CCR8 full-length protein-synthetic nanodisc | |
| FC验证抗体 | DME100180 | Anti-CCR8 antibody(DM180); Rabbit mAb |
| DME100195 | Anti-CCR8 antibody(DM195); Rabbit mAb | |
| DME100196 | Anti-CCR8 antibody(DM196); Rabbit mAb | |
| DME100197 | Anti-CCR8 antibody(DM197); Rabbit mAb | |
| 参照抗体 | BME100063 | Anti-CCR8(10A11) mAb |
| BME100115 | Anti-CCR8(BMS 986340) mAb | |
| 生物素标记抗体 | DME100180B | Biotinylated Anti-CCR8 antibody(DM180); Rabbit mAb |
| DME100195B | Biotinylated Anti-CCR8 antibody(DM195); Rabbit mAb | |
| DME100196B | Biotinylated Anti-CCR8 antibody(DM196); Rabbit mAb | |
| DME100197B | Biotinylated Anti-CCR8 antibody(DM197); Rabbit mAb | |
| BME100063B | Biotinylated Anti-CCR8(10A11) mAb | |
| BME100115B | Biotinylated Anti-CCR8(BMS 986340) mAb |
参考文献:
[1] Korbecki J , Grochans S , Gutowska I , et al. Cc chemokines in a tumor: A review of pro-cancer and anti-cancer properties of receptors ccr5, ccr6, ccr7, ccr8, ccr9, and ccr10 ligands[J]. International Journal of Molecular Sciences, 2020, 21(20):1-34.

