在肿瘤治疗的博弈中,“铁死亡”(Ferroptosis)正成为击破耐药肿瘤的突破口。恶性肿瘤虽通过代谢重塑维持高增殖,却也因此背负了沉重的氧化应激负荷。这种天然的代谢脆弱性,迫使肿瘤细胞高度依赖一套严密的防御系统,而溶质载体家族7成员11(Solute Carrier Family 7 Member 11,SLC7A11),亦称xCT,正是这道防线上最关键的守门人。作为System xc–(一种异二聚体氨基酸转运蛋白复合物)的核心亚基,SLC7A11介导的胱氨酸摄取是合成抗氧化剂谷胱甘肽(GSH)的限速步骤,直接决定了肿瘤抵御铁死亡的能力。2025年初,《Cell》与《Nature》等顶刊研究指出,SLC7A11既是肿瘤生存的保障,也可能在特定条件下诱发双硫死亡(Disulfidptosis) [1][2]。这种从盾到矛的角色切换,使其成为当下最具潜力的广谱抗癌靶点之一。本文将从SLC7A11的蛋白结构出发,深度解析其在铁死亡中的调控机制及最新的临床研究进展。
一、SLC蛋白家族与SLC7A11
SLC7A11是人体重要的氨基酸转运蛋白,隶属于溶质载体(SLC)蛋白家族中的SLC7亚家族。SLC蛋白家族是人体最大的膜转运蛋白家族之一,涵盖400余种转运体,分为60余个亚家族,广泛参与氨基酸、葡萄糖、核苷酸、离子及代谢物的跨膜运输。典型成员包括葡萄糖转运蛋白SLC2家族(如GLUT1、GLUT4)、中性氨基酸转运体SLC1家族(如SLC1A5)、阳离子氨基酸转运体SLC7家族(如SLC7A11)以及乳酸转运体SLC16家族等。这些转运蛋白在代谢调控、神经信号传导、肿瘤营养依赖和药物摄取中发挥关键作用,是当前代谢类与肿瘤类药物研发的重要靶点来源。
在SLC7家族中,根据结构与功能差异可分为阳离子氨基酸转运体(CATs)和轻链氨基酸转运体(LATs)两大类,SLC7A11属于后者,是典型的多跨膜整合膜蛋白,由约501个氨基酸组成,包含12个跨膜螺旋结构。其N端与C端均位于胞质侧,中间跨膜区形成底物结合和交换通道。
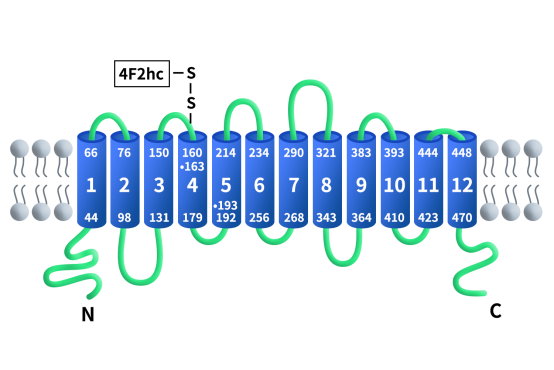
Figure 1. The structure of SLC7A11/xCT [3]
二、SLC7A11分布与功能
在正常生理状态下,SLC7A11在脑组织(小胶质细胞、星形胶质细胞)和免疫细胞中表达相对较高。但在多种恶性肿瘤(如非小细胞肺癌、胰腺癌、胶质瘤、乳腺癌)中,受NRF2等转录因子的驱动,SLC7A11呈现高度过表达态势,成为肿瘤细胞应对氧化应激的保护伞。如前所述,SLC7A11是system xc–逆向转运系统的功能亚基。该系统由轻链SLC7A11与重链SLC3A2(CD98hc)通过二硫键形成异源二聚体,共同定位于细胞膜,二硫键位于SLC7A11的158位保守残基Cys和SLC3A2的109位Cys之间。SLC3A2是一种单次跨膜蛋白,作为分子伴侣维持SLC7A11蛋白的稳定性和适当的膜定位,而SLC7A11负责底物特异性识别和转运功能。
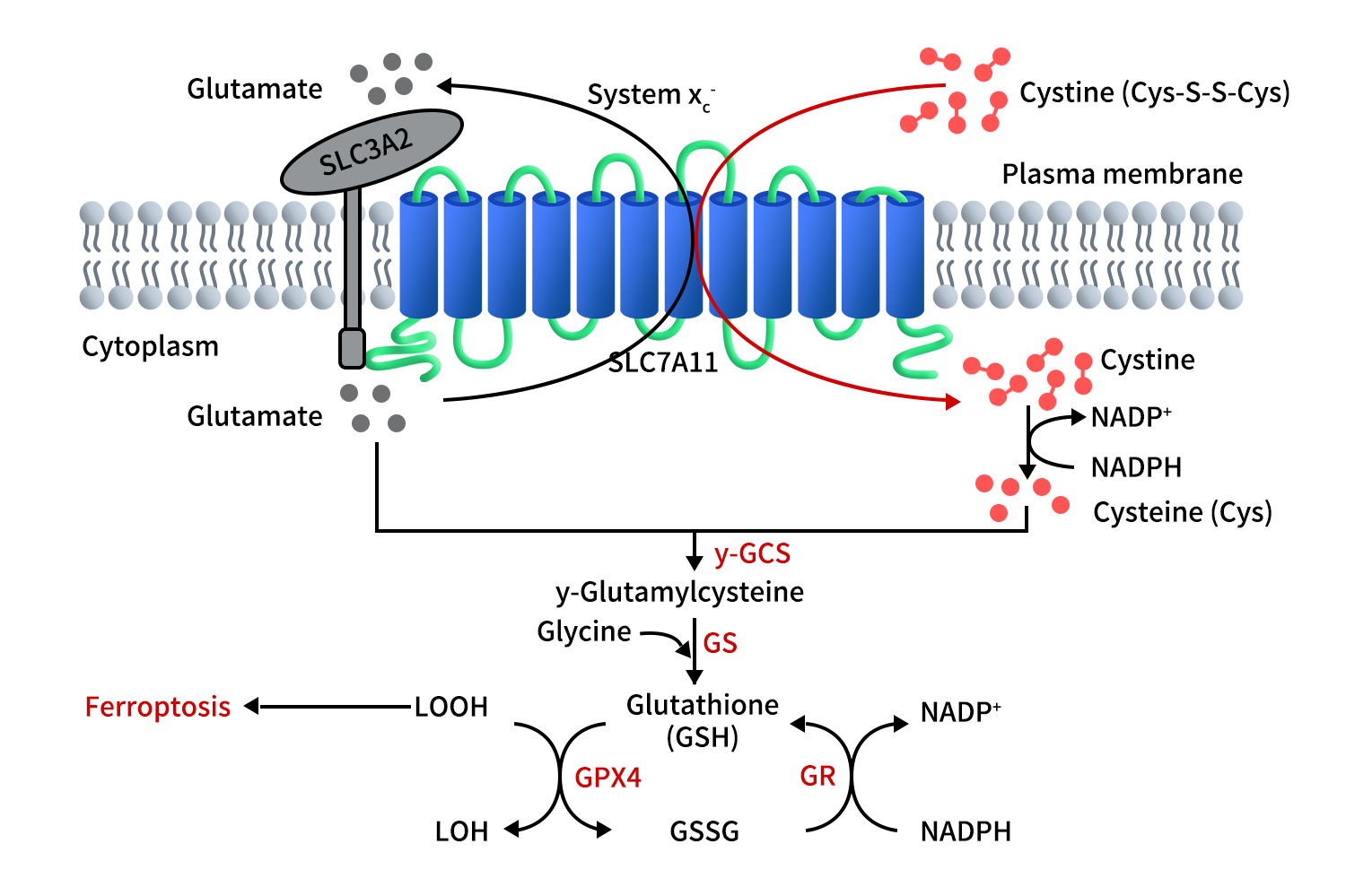
Figure 2. The function of SLC7A11 [3]
SLC7A11通过1:1等摩尔比交换细胞外胱氨酸与胞内谷氨酸,实现半胱氨酸供给,从而支持GSH合成,维持细胞氧化还原稳态。如上图所示,首先胞外胱氨酸通过SLC7A11进入细胞,然后通过消耗NADPH的还原反应转化为半胱氨酸。随后,半胱氨酸通过两步法合成GSH。第一步,半胱氨酸在γ-谷氨酰半胱氨酸合物(γ-GCS)的催化下与谷氨酸结合形成 γ-谷氨酰半胱氨酸。第二步,GS介导的酶促反应将甘氨酸分子添加到γ-谷氨酰半胱氨酸上,生成GSH。细胞膜中脂质过氧化物的过度积累会诱导铁死亡。谷胱甘肽过氧化物酶4(GPX4)利用GSH将脂质过氧化物还原为脂质醇,从而抑制铁死亡。在此过程中,GSH被氧化为GSSG;GSSG随后通过GR介导的还原反应(消耗NADPH)还原回GSH。
三、SLC7A11在肿瘤细胞中的作用机制
肿瘤细胞通常处于高氧化应激与高代谢状态,对抗氧化系统高度依赖,因此SLC7A11通过维持GSH水平成为肿瘤生存与增殖的重要代谢支撑。
在铁死亡调控方面,SLC7A11处于关键上游节点。GSH是GPX4的辅因子,后者负责还原脂质过氧化物,阻止膜脂质过氧化积累。当SLC7A11被抑制或表达下调时,GSH耗竭、GPX4活性下降,脂质ROS积累,最终触发铁依赖性的细胞死亡。因此,SLC7A11被视为铁死亡敏感性的决定因素之一,也是近年来抗肿瘤代谢治疗的重要干预靶点。
在信号调控层面,SLC7A11受到多条肿瘤相关通路调控。抑癌基因p53可通过转录抑制SLC7A11表达,从而增强细胞对铁死亡的敏感性;而NRF2在氧化应激条件下可上调SLC7A11转录,促进抗氧化防御。此外,ATF4、MYC等代谢相关转录因子亦可增强其表达,帮助肿瘤细胞在营养匮乏或治疗压力下维持还原环境。这种“代谢依赖—氧化保护”轴线使SLC7A11成为肿瘤耐药的重要分子基础,例如在化疗、放疗及部分靶向治疗过程中,SLC7A11上调可降低治疗诱导的ROS损伤。此外,SLC7A11外排谷氨酸还可能改变肿瘤微环境,影响免疫细胞与神经相关信号通路。在胶质瘤等肿瘤中,过量谷氨酸释放与肿瘤侵袭性增强相关 [3][4][5][6]。
近年来,甘培学等教授在2023-2024年的研究中揭示了一个有趣的现象:虽然SLC7A11能防范铁死亡,但在葡萄糖缺乏的情况下,极高水平的SLC7A11会导致胞内胱氨酸及其他双硫化物过度积累。由于缺乏还原当量(NADPH),过剩的双硫化物会引起肌动蛋白细胞骨架的塌陷,诱发一种独特的死亡方式,即双硫死亡。这一发现为开发“诱导 SLC7A11 高表达+代谢抑制”的联合疗法提供了理论依据[7] [8]。
四、SLC7A11药物临床药物研究进展
SLC7A11异常表达与多种疾病密切相关,尤其在肿瘤中显著上调,如胰腺癌、三阴性乳腺癌、肺癌、肝细胞癌及胶质瘤等,常与肿瘤进展及不良预后相关。在阿尔茨海默病、缺血再灌注损伤等疾病中,SLC7A11也参与氧化应激调控。由于其处于氧化还原失衡与代谢重编程的关键节点,逐渐成为重要治疗靶点。尽管SLC7A11的重要性不言而喻,但目前仍缺乏高选择性的上市药物。现有的策略主要分为以下几类:
4.1 传统小分子抑制剂
柳氮磺胺吡啶(Sulfasalazine),最初由Pfizer等企业开发并上市,用于类风湿关节炎和炎症性肠病治疗。后续研究发现其可抑制SLC7A11介导的胱氨酸摄取,从而诱导铁死亡。该药是目前唯一进入临床评价的SLC7A11抑制剂,但由于药代动力学性质差、选择性低,在临床试验中表现平平。
索拉非尼(Sorafenib),由Bayer开发,是已上市的多激酶抑制剂,用于肝细胞癌和肾癌治疗。后续机制研究发现其部分抗肿瘤活性可能涉及ferroptosis通路调控,并间接影响SLC7A11相关代谢轴。不过,索拉非尼并非选择性SLC7A11抑制剂,其铁死亡效应更多属于机制拓展发现,而非专门靶向开发。
4.2 下一代高选择性小分子
- FC-001是目前全球少数真正进入临床阶段的选择性SLC7A11抑制剂之一,由日本生物技术公司FerroptoCure研发。该药已推进至I期临床,主要针对晚期实体瘤进行安全性与初步疗效评估,被视为潜在“first-in-class”铁死亡靶向分子,整体仍处于早期临床验证阶段。
- Erastin及其改良衍生物(如IKE)最早由Columbia University等学术团队发现,是经典的铁死亡诱导分子。Erastin能够直接抑制SLC7A11功能,但因体内稳定性和溶解性较差未能进入临床。后续开发的Imidazole Ketone Erastin通过结构优化改善药代性质,目前仍处于临床前阶段。
在传统小分子抑制剂之外,针对 SLC7A11的新兴技术路线正在逐步展开,尤其是PROTAC蛋白降解策略和肿瘤疫苗方向,体现出从功能抑制向蛋白清除和免疫中和延伸的趋势,但均处于早期研发阶段,尚未有重大突破。
五、缔码生物SLC7A11 nanodisc产品助力SLC7A11药物研发
尽管目前针对SLC7A11的药物开发已出现小分子、疫苗等多种策略,但所有机制研究与药物筛选都离不开高质量的SLC7A11膜蛋白。全长SLC7A11结构复杂、跨膜区众多,传统可溶片段或细胞膜粗提物难以满足结构解析、结合位点验证及药筛需求。因此,能稳定呈现天然构象的SLC7A11 nanodisc全长膜蛋白,正成为开展机理研究与先导化合物评估的关键工具。
缔码生物利用其哺乳动物细胞表达系统已成功制备了具有天然构象与完整跨膜结构的全长 SLC7A11,该蛋白可在无去垢剂环境中保持天然构象与翻译后修饰,为结构分析、抗体筛选与药物结合测试提供更可靠的靶点模型,正逐渐成为药物研发早期的重要资源。
Human SLC7A11 full length protein-synthetic nanodisc (FLP100048)
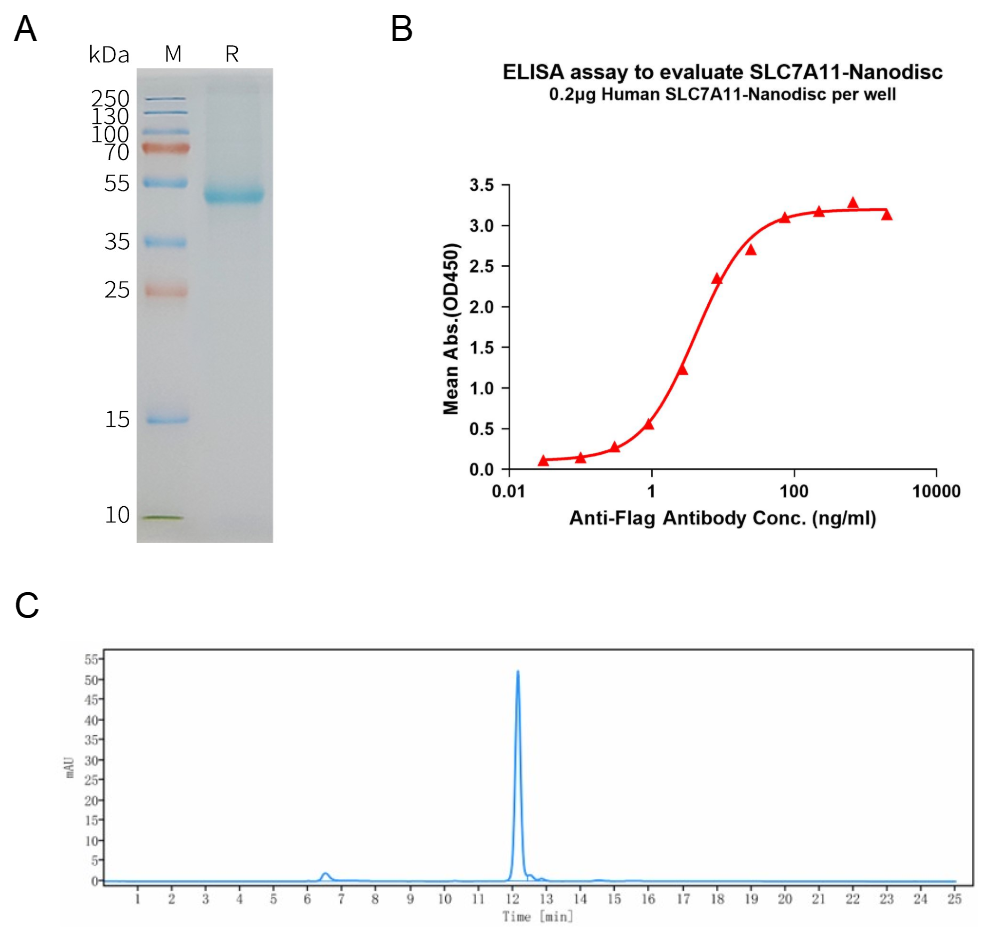
A: Human SLC7A11-Nanodisc, Flag Tag on SDS-PAGE;
B: ELISA analysis of SLC7A11-Nanodisc can bind with anti-Flag monoclonal antibody and the EC50 is 4.101ng/ml;
C: The purity of Human SLC7A11-Nanodisc is greater than 90% as determined by SEC-HPLC.
Reference:
- Chen, X., et al. (2025). “Ferroptosis 2025: Decade of discovery and the future of therapy.” Cell.
- Gan, B., et al. (2024). “The multifaceted role of SLC7A11 in cancer: from ferroptosis to disulfidptosis.” Nature Reviews Cancer.
- Koppula P, Zhuang L, Gan B. Cystine transporter SLC7A11/xCT in cancer: ferroptosis, nutrient dependency, and cancer therapy. Protein Cell. 2021 Aug;12(8):599-620.
- Dixon SJ, et al. Ferroptosis: an iron-dependent form of nonapoptotic cell death. Cell. 2012.
- Jiang L, et al. Ferroptosis as a p53-mediated activity during tumour suppression. Nature. 2015.
- Liu X, et al. Cystine transporter regulation of redox balance in cancer. Trends in Cancer. 2020.
- Liu, X., et al. (2023). “Actin cytoskeleton vulnerability to disulfide stress mediates disulfidptosis.” Nature Cell Biology.
- Zheng, J., et al. (2024). “SLC7A11-mediated metabolism: a double-edged sword in cancer.” Cell Death & Disease.


