人癌胚抗原相关的细胞粘附分子5(CEACAM5)是一种肿瘤特异性抗原,由Gold和Freeman于1965年首次在结肠癌中发现 [1] [2]。一直以来,CEACAM5作为结直肠癌临床诊疗中常用的肿瘤标志物来帮助诊断和检测肿瘤发展。近几年随着研究的深入,CEACAM5作为肿瘤靶点用于新药开发的潜能也逐步凸显出来。2023年AACR会议上,赛诺菲和礼新医药分别公布了其CEACAM5 ADC和双抗的在研进展。那CEACAM5究竟什么?表达有何特点?目前布局CEACAM5靶点的管线又有哪些?涉及哪些适应症?
1、CEACAM5的结构与分布
CEACAMs分子属于免疫球蛋白超家族黏附分子,是一类细胞表面糖蛋白家族,共包含12个家族成员,分别是CEACAM1、CEACAM3、CEACAM4、CEACAM5、CEACAM6、CEACAM7、CEACAM8、CEACAM16、CEACAM18、CEACAM19、CEACAM20和CEACAM21。除CEACAM16外,其他CEACAMs蛋白分子N端都有一个108个氨基酸组成的免疫球蛋白可变区(IgV)样结构域,而CEACAM16蛋白N端有两个。不过,它们N端的免疫球蛋白恒定区(IgC)2型样结构域数量从0-6个不等。虽然所有CEACAMs分子都连接在细胞膜上,但不同的是,CEACAM5、CEACAM6、CEACAM7和CEACAM8是通过GPI连锁与细胞膜结合,而CEACAM1、CEACAM3、CEACAM4、CEACAM19、CEACAM20和CEACAM21是通过跨膜结构域锚定在细胞膜上。CEACAM16是无膜锚定的分泌型。
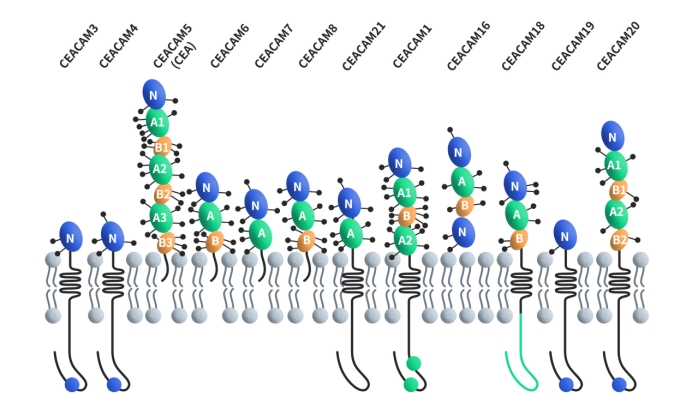
Figure 1. The structures of CEACAMs [4]
CEACAM5,也称为CEA(癌胚蛋白)或CD66e,是癌胚抗原相关细胞粘附分子(CEACAMs)家族的首位成员。人源CEACAM5基因位于染色体19q13.2,基因长度约为 21 kb,由9个外显子和3个非编码外显子组成。CEACAM5蛋白由642个氨基酸组成(分子量约为70kDa),具有 28 个潜在的 N 连接糖基化位点。一个CEACAM5蛋白分子中含有24-26个天冬酰胺连接的糖链,其最终分子量约为180kDa。该蛋白通过糖基磷脂酰肌醇(GPI)与膜结合,胞外共有7个免疫球蛋白样结构域,包括一个是可变(lgV)样结构域和6个lgC样结构域(A1-B3),lg结构域前有一个34个氨基酸的信号肽 [3] [4]。
与其他在造血细胞中表达CEACAMs分子(如CEACAM1、CEACAM8、CEACAM6等)相比,尚未在造血细胞中检测到CEACAM5的表达。相关研究表明,CEACAM5的表达始于人类胚胎和胎儿发育的早期阶段(9-14周),并在某些细胞中保持终身表达。在成人正常组织中,CEACAM5主要存在于结肠柱状上皮细胞和杯状细胞中,也存在于胃、舌、食道、宫颈、汗腺和前列腺中 [5]。值得注意的是,正常情况下,肺和胃肠道上皮细胞中CEACAM5的表达仅限于上皮细胞膜面向腔内的顶端表面,所以不能被免疫细胞识别。
2、CEACAM5与癌症
在癌细胞中,CEACAM5主要在上皮肿瘤细胞表面高表达,包括结直肠癌、胃癌、胰腺癌、胆囊癌、肺腺癌、小细胞肺癌、乳腺癌、膀胱癌、卵巢癌等。
2.1、 CEACAM5与结直肠癌
CEACAM5在超80%的结直肠癌(CRC)中表达,目前已经广泛用作CRC的预后标志物。现已明确的是,术前CEACAM5水平升高的患者生存结果较差 [6]。有研究表明,CEACAM5的强制过度表达与失巢凋亡(一种由细胞基质脱离引起的细胞凋亡形式)相关,会增强癌细胞转移 [7]。复旦大学上海肿瘤中心结直肠外科蔡三军团队研究表明结直肠癌转移可通过FBW7以HIF1α依赖性方式调控CEACAM5的表达抑制 [8]。
2.2、CEACAM5与胃肠癌
CEACAM5在约90%的胃肠癌(GC)中过度表达,其过度表达可以改变细胞极性和正常组织结构,减缓细胞分化和成熟,最终导致肿瘤形成 [9]。2015年,第四军医大学西京消化病医院肿瘤生物学国家重点实验室聂永战团队鉴定出MGd1的抗原是CEACAM5,并利用MGd1研究CEACAM5在非GC和GC组织中的表达。他们的研究结果表明,CEACAM5的表达从正常胃黏膜到慢性萎缩性胃炎、肠上皮化生、不典型增生直至GC逐渐升高。在胃癌前病变(肠化生和不典型增生)中,CEACAM5阳性患者比CEACAM5阴性患者发生GC的风险更高。此外,CEACAM5与胃腺癌的浸润深度呈正相关。基于这些结果,团队认为CEACAM5可作为胃癌预警和预后的生物标志物 [10]。2022年,江汉大学附属武汉市第六医院消化外科刘念团队就CEACAM5在胃癌中上游调控通路开展了研究。研究结果证明了CEACAM5在促进GC细胞迁移、增殖和EMT中的作用。此外,团队还发现miR-498能够通过下调CEACAM5来控制GC细胞的生长 [11]。
2.3、CEACAM5与非小细胞肺癌
CEACAM5约在20%的NSCLC腺癌患者中高表达。2020临沂市中心医院Xinwen Zhang等人通过qRT-PCR发现,CEACAM5在NSCLC组织和细胞系中表达升高;利用IHC分析87 名患者肿瘤中CEACAM5的表达发现,CEACAM5的表达与肿瘤分期、淋巴侵袭和组织学分级显着相关。此外,这项研究中的体外实验证实CEACAM5可通过抑制p38-SMAD2/3信号通路来刺激NSCLC细胞增殖和迁移[9]。
3、靶向CEACAM5临床管线研究进展
在临床开发方面,研究人员正在全面开发CEACAM5作为多种新型治疗靶点的生物疗法,包括 ADC、双特异性抗体和嵌合抗原受体 T 细胞疗法。这些研究大部分集中在结直肠癌和其他胃肠道恶性肿瘤上。据不完全统计,目前处于临床前或临床阶段的靶向CEACAM5疗法大约有25项,其中12项单抗、5项ADC、3项双特异性抗体、5项car-t疗法。这里重点展示了进入临床阶段的几项疗法。
3.1、tusamitamab ravtansine
Tusamitamab ravtansine(代号:SAR408701)是Sanofi从ImmunoGen引进的一款新型抗体偶联药物(ADC),这款ADC由抗CEACAM5人源化单克隆抗体和DM4通过ImmunoGen开发的可切割链接子(SPDB)偶联而成。DM4是细胞毒性美登木素生物碱,可特异性靶向表达CEACAM5的肿瘤细胞。目前处在临床III期,针对的主要适应症为非小细胞肺癌。
正在进行的II期临床试验CARMEN-LC05研究旨在评估tusamitamab ravtansine在双联(+Keytruda)、三联(+Keytruda+含铂化疗)和四联(+Keytruda+含铂化疗+培美曲塞)组合疗法在晚期/转移性非鳞状NSCLC患者中的疗效和安全性。在所有治疗组中,患者每3周接受 150 mg/m2或170 mg/m2的tusamitamab ravtansine静脉注射。在所有剂量水平中,总体缓解率(ORR)为52%,中位治疗持续时间为24.3周。而且36%的患者病情稳定,12%的患者病情进展,疾病控制率为88%。在所有PDL1表达水平组均观察到应答,在CEACAM5中/高表达组均观察到应答,双联组的疗效尤其突出 [12]。
3.2、Labetuzumab govitecan
Labetuzumab govitecan(IMMU-130)是Immunomedics开发的一款ADC药物,由抗CEACAM5单克隆抗体和SN-38通过PH敏感型连接子组成。SN-38是抗肿瘤药伊立替康的活性代谢物。目前处在临床II期,针对的适应症主要是结直肠癌。
2017年8月17日,刊登在《J Clin Oncol》杂志上的1/2期试验研究评估了Labetuzumab govitecan治疗复发或难治性转移性结直肠癌(mCRC)的效果。该项试验研究入组了86例难治性结直肠癌患者(之前平均已经接受过5次治疗),这些患者每周接受一次8和10 mg/kg 的Labetuzumab govitecan治疗,或在每个周期(以3周为一个周期)的第1周和第2周每周接受两次4和6 mg/kg 的Labetuzumab govitecan治疗。结果表明38%的患者出现了不同程度的肿瘤缩小。一名患者取得了部分缓解,且持续缓解超过2年,42名患者达到了疾病稳定,中位总生存期为6.9个月。这表明labetuzumab govitecan 单药治疗显示出可控的安全性和治疗活性 [13]。
3.3、cibisatamab
Cibisatamab是罗氏开发的CEACAM5xCD3双特异性抗体,是一种T细胞双特异性抗体,结合癌细胞上的CEACAM5(又称CEA)和T细胞上的CD3。该结构使得Cibisatamab的一只“手臂”附着在CEACAM5上,另一只手臂将T细胞拉过来并激活,促使其攻击肿瘤。Cibisatamab在T细胞上有1个CD3ε链的单结合位点和2个CEA结合位点。目前处于临床II期研究,针对的适应症主要是结直肠癌。罗氏临床开发并没有采用cibisatamab单药,当前进行的临床I/II期试验共有两项,一项(NCT04826003)是将FAP/4-1BB双抗RO7122290(共刺激双抗)与cibisatamab联用,另一项(NCT03866239)是将 PD-L1单抗atezolizumab(T药)与cibisatamab联用。研究人群是既往接受过治疗的转移性、微卫星稳定、CEACAM5高表达的结直肠腺癌患者。目前,二者研究均处于招募中。
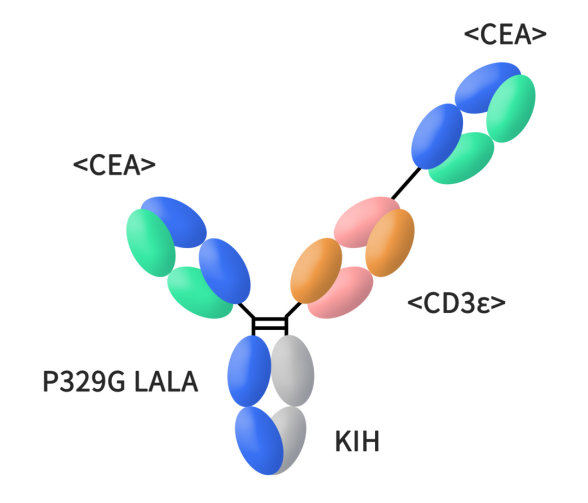
Figure 2. The structure of cibisatamab
3.4、MG7-CAR-T
MG7是糖基化CEACAM5蛋白,是一种具有高特异性和敏感性的胃癌相关性抗原。MG7-CART是由吉凯基因开发的抗MG7抗体改造嵌合抗原受体疗法。吉凯基因在2017年AACR会议上展示的结果表明MG7-CART在胃癌肿瘤病人的PDX模型中能够显著抑制PDX肿瘤生长并清除了60%小鼠的肿瘤,治疗效果显著。目前处于临床II期研究,针对的适应症主要是结直肠癌和胃癌。
4、缔码CEACAM5蛋白抗体助力CEACAM5靶向药物研发
缔码生物是一家专注于提供可成药靶点临床前研发产品和服务的生物技术公司。公司拥有创新型功能膜蛋白开发、单B细胞先导抗体发现、抗体工程改造与功能验证平台,旨在让药企跨过单抗平台建立和先导分子筛选的门槛,加速推进临床管线。针对CEACAM5靶点,缔码生物提供CEACAM5靶点全系列产品及服务,包括以现货形式提供的活性蛋白、兔单抗和阳参抗体。此外,针对CEACAM5靶点,我司还构建了CAR分子,并完成了CAR分子体外验证实验,以上产品均可满足CEACAM5抗体药相关研究。
4.1、CEACAM5活性蛋白
Human CEACAM5 Protein, His Tag (PME100071)
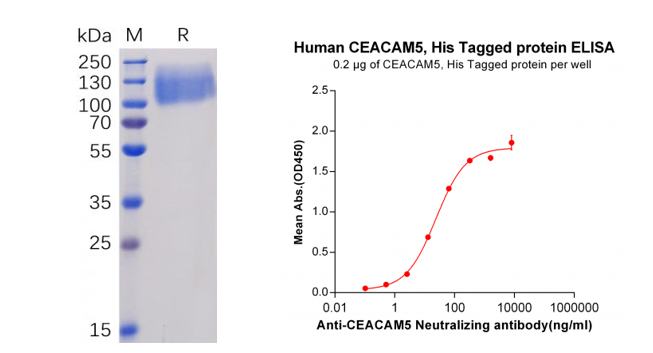
Figure 3. Validation data of purified Human CEACAM5 Protein, His Tag (PME100071). Human CEACAM5 Protein, His Tag on SDS-PAGE (left); CEACAM5 Protein (PME100071) can bind Anti-CEACAM5 Antibody (BME100035) in a linear range of 2.56-320 ng/ml (right).
4.2、CEACAM5兔单抗
Anti-CEACAM5 antibody(DM120); Rabbit mAb (DME100120)
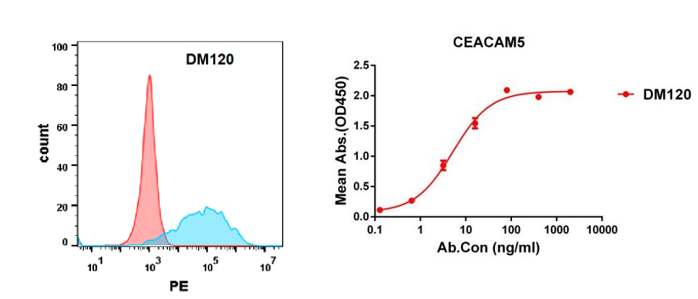
Figure 4. Validation data of Anti-CEACAM5 antibody(DM120) Rabbit mAb (DME100120). Flow cytometry analysis with Anti-CEACAM5 (DM120) on HEK293 cells transfected with human CEACAM5(Blue) or irrelevant protein (Red) (left). Anti-CEACAM5 antibody(DM120) (DME100120) can bind His tagged protein (PME100071) in a linear range of 0.1-50 ng/ml (right).
此外,缔码已成功制备CEACAM5单B细胞种子库,最快20天可实现更多CEACAM5先导抗体分子筛选,点击了解更多缔码B细胞种子库>>
4.3、CEACAM5参照抗体
Anti-CEACAM5 (labetuzumab biosimilar) mAb (BME100035)
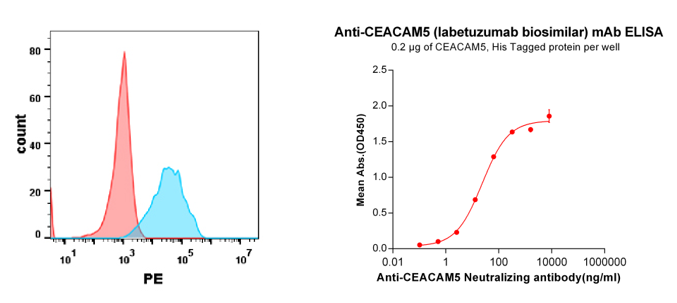
Figure 5. Validation data of Anti-CEACAM5 (labetuzumab biosimilar) mAb (BME100035); Flow cytometry analysis with Anti-CEACAM5 (labetuzumab) on HEK293 cells transfected with human CEACAM5 (Blue) or HEK293 transfected with irrelevant protein(Red) (left). His tagged protein (PME100071) can bind Anti-CEACAM5 Neutralizing antibody(BME100035) in a linear range of 2.56-320 ng/ml (right).
4.4、CEACAM5抗体人源化服务
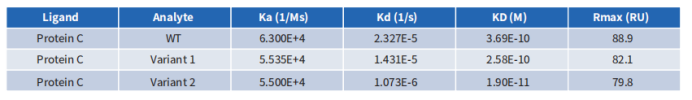
采用通用模板进行人源化,CEACAM5抗体亲和力完全丢失;采用缔码人源化抗体库进行筛选后,获得比嵌合抗体亲和力更高的克隆。
4.5、CEACAM5 CAR分子体外杀伤试验
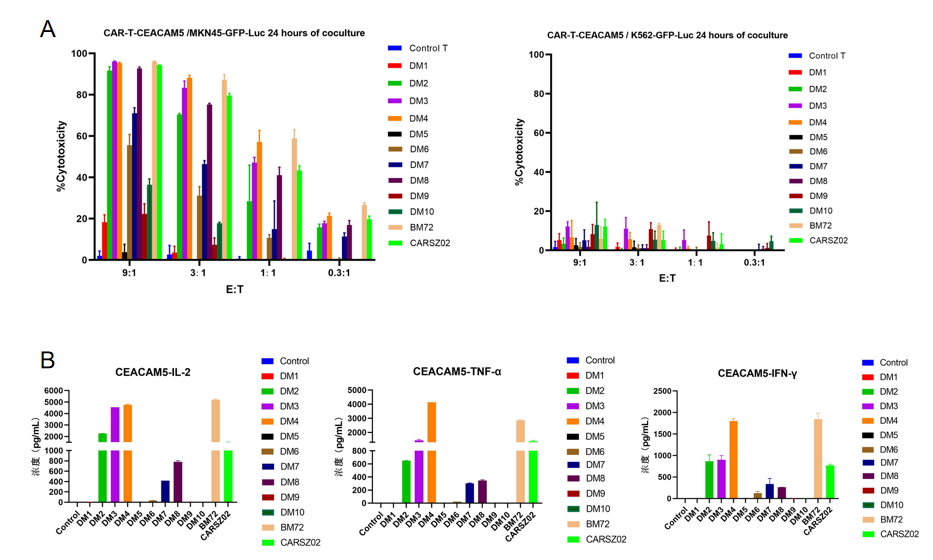
Figure 6. 24-hour in vitro killing test of CEACAM5 CAR T cells carrying humanized scFv constructs developed by DIMA. The results show that most of these CAR T cells effectively killed MKN-45 cells (naturally expressing CEACAM5) while not killing K562 cells (negative control). IL-2, TNF-α, and IFN-γ were detected 24 hours after the killing experiment at the effect target ratio of 3:1.
4.6、产品列表
参考文献
[1] Gold, P. and Freedman, S.O. (1965) Demonstration of Tu-mor-Specific Antigens in Human Colonic Carcinomata by Immunological Tolerance and Absorption Techniques. Journal of Experimental Medicine, 121, 439-462.
[2] Gold, P. and Freedman, S.O. (1965) Specific Carcinoembryonic Anti-gens of the Human Digestive System. Journal of Experimental Medicine, 122, 467-481.
[3] Beauchemin, N., Draber, P., Dveksler, G., Gold, P., Gray-Owen, S., Grunert, F., et al. (1999). Redefined nomenclature for members of the carcinoembryonic antigen family. Experimental Cell Research, 252(2), 243–249.
[4] Beauchemin N, Arabzadeh A. Carcinoembryonic antigen-related cell adhesion molecules (CEACAMs) in cancer progression and metastasis. Cancer Metastasis Rev. 2013 Dec;32(3-4):643-71.
[5] Nap M, Mollgard K, Burtin P, Fleuren GJ. Immunohistochemistry of carcino-embryonic antigen in the embryo, fetus and adult. Tumour Biol. 1988;9(2-3):145-53.
[6] Thirunavukarasu P, Sukumar S, Sathaiah M, Mahan M, Pragatheeshwar KD, Pingpank JF, et al. C-stage in colon cancer: implications of carcinoembryonic antigen biomarker in staging, prognosis, and management. Journal of the National Cancer Institute. 2011; 103: 689-97.
[7] Ordonez C, Screaton RA, Ilantzis C, Stanners CP. Human carcinoembryonic antigen functions as a general inhibitor of anoikis. Cancer research. 2000; 60: 3419-24.
[8] Li Q, Li Y, Li J, Ma Y, Dai W, Mo S, Xu Y, Li X, Cai S. FBW7 suppresses metastasis of colorectal cancer by inhibiting HIF1α/CEACAM5 functional axis. Int J Biol Sci. 2018 May 12;14(7):726-735.
[9] Zhang X, Han X, Zuo P, Zhang X, Xu H. CEACAM5 stimulates the progression of non-small-cell lung cancer by promoting cell proliferation and migration. J Int Med Res. 2020 Sep;48(9):300060520959478.
[10] Zhou J, Fan X, Chen N, Zhou F, Dong J, Nie Y, Fan D. Identification of CEACAM5 as a Biomarker for Prewarning and Prognosis in Gastric Cancer. J Histochem Cytochem. 2015 Dec;63(12):922-30.
[11] Zhang L, Zhang C, Liu N. CEACAM5 targeted by miR-498 promotes cell proliferation, migration and epithelial to mesenchymal transition in gastric cancer. Transl Oncol. 2022 Oct;24:101491.
[12] Paz-Ares L, Nagy T, Ravoire M, et al. Safety and efficacy of tusamitamab ravtansine in comination with pembrolizumab ± chemotherapy in patients with CEACAM5-positive nonsquamous NSCLC (CARMEN-LC05 phase 2 study). Presented at: 2023 European Lung Cancer Congress; March 29-April 1, 2023; Copenhagen, Denmark. Abstract 13MO.
[13] Dotan E, Cohen SJ, Starodub AN, Lieu CH, Messersmith WA, Simpson PS, Guarino MJ, Marshall JL, Goldberg RM, Hecht JR, Wegener WA, Sharkey RM, Govindan SV, Goldenberg DM, Berlin JD. Phase I/II Trial of Labetuzumab Govitecan (Anti-CEACAM5/SN-38 Antibody-Drug Conjugate) in Patients With Refractory or Relapsing Metastatic Colorectal Cancer. J Clin Oncol. 2017 Oct 10;35(29):3338-3346.


