过去几年,血脑屏障(blood-brain barrier,BBB)递送已从概念验证迈向临床验证。2025年7月,Roche的trontinemab数据显示,在3.6 mg/kg剂量下,28周后91%受试者实现amyloid PET阴性,且ARIA-E低于5%,再次验证了BBB穿梭策略的临床潜力[1]。同时,AbbVie收购Aliada Therapeutics,将BBB穿透技术明确纳入核心交易逻辑[2];更早前,JCR的pabinafusp alfa已在日本获批上市,成为该领域商业化标杆[3]。这些进展表明,BBB正从开发障碍转变为神经系统药物竞争力的关键入口。在正是介绍BBB穿梭机制之前,我们先简单说下什么是血脑屏障。
一、什么是血脑屏障BBB?
如图所示,血脑屏障(BBB)是一种高度复杂且动态调控的结构,其核心由具备紧密连接的脑微血管内皮细胞(ECs)构成,并由基底膜、星形胶质细胞、周细胞及细胞外基质(ECM)共同支撑。其主要功能位点位于脑毛细血管,是血液与脑组织物质交换的关键界面,总表面积约达12–18 m²,使其成为体内最大的血–脑交换界面。除BBB外,脑内还存在血–脑脊液屏障(BCSFB)及蛛网膜屏障,但后者因无血管且表面积较小,对物质交换贡献有限。
BBB的功能依赖于神经血管单元(NVU)的协同作用,包括内皮细胞、星形胶质细胞、周细胞等。其中,星形胶质细胞通过足突覆盖毛细血管并分泌多种调控因子,维持内皮细胞稳定性;周细胞则环绕内皮细胞,提供结构支持并调控通透性与血流。周细胞在不同血管区域具有功能差异:动脉侧参与血流调节,静脉毛细血管侧则更偏向维持屏障完整性与免疫调控。
正是内皮细胞、星形胶质细胞与周细胞之间的协同作用,共同维持了BBB的结构稳定性和选择性通透功能。
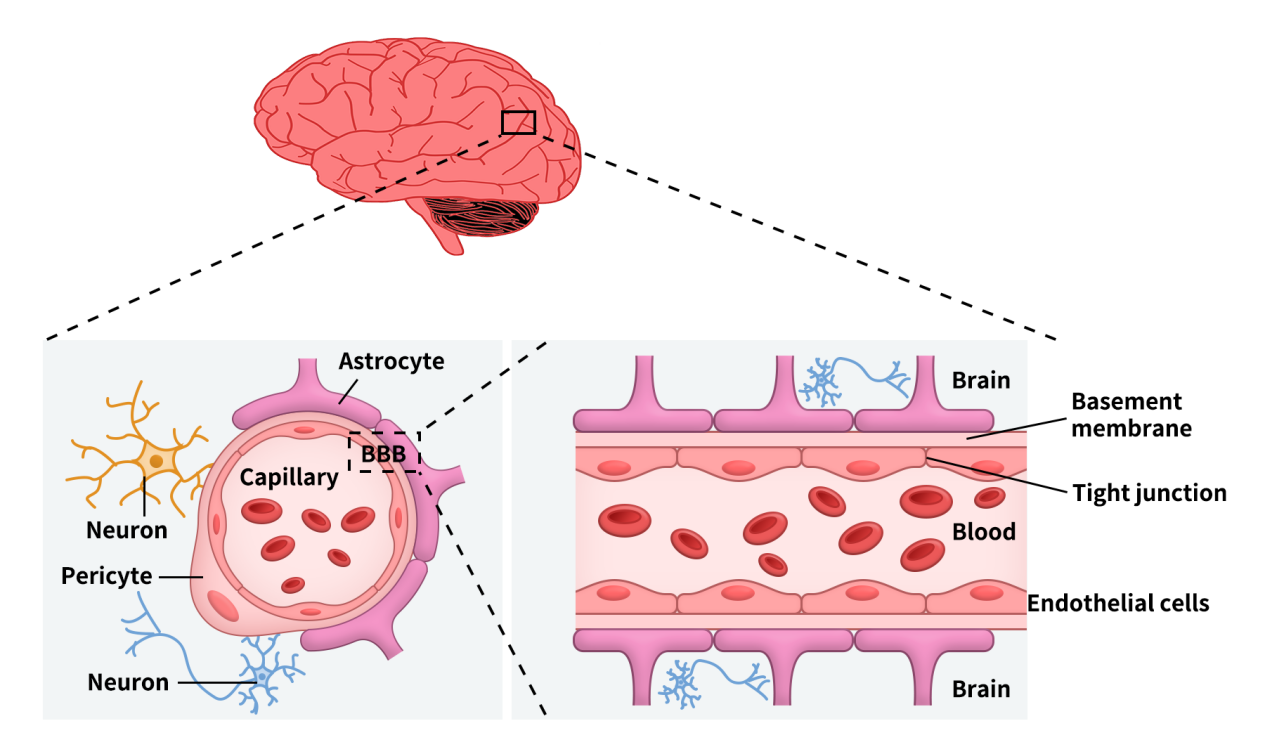
Figure 1. Blood-brain barrier (BBB) components and composition [4]
二、BBB穿梭机制概述
从研发角度看,关于BBB穿梭药物开发,目前问题已不再是“能否过BBB”,而是“通过何种机制进入”。目前主流路径主要包括三类:受体介导跨胞转运(receptor-mediated transcytosis,RMT)、转运体介导运输(carrier-mediated transport,CMT)以及吸附介导跨胞转运(adsorptive-mediated transcytosis,AMT)[4,5]。
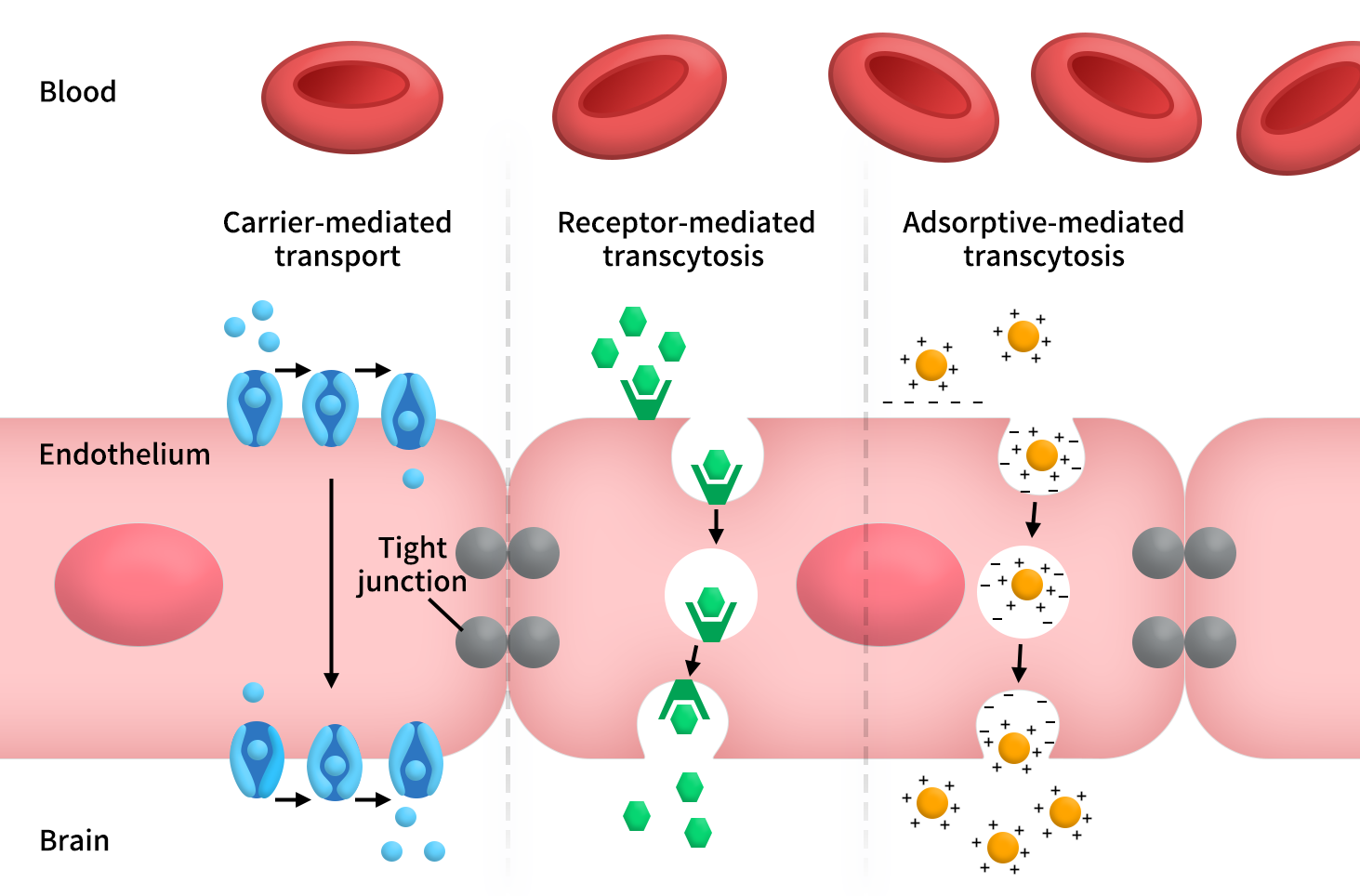
Figure 2. Three main ways through the BBB
其中,RMT是最成熟、最接近平台化的一条主线。其核心逻辑是让药物首先识别BBB内皮表面的特定受体,随后通过受体介导内吞、胞内分选和跨胞外排进入脑实质。由于这一机制天然适合搬运大分子货物,因此抗体、酶替代药物、双特异性抗体、融合蛋白乃至部分核酸偶联物,往往最优先考虑RMT路径。与RMT更适合生物大分子不同,CMT更适合小分子、前药和结构伪装策略。其基本逻辑是借用BBB对葡萄糖、氨基酸、单羧酸等营养物质的天然摄取系统,让药物“伪装成底物”进入中枢。此外,AMT也是BBB研究中经常被提到的一类路径。它主要依赖带正电的肽、蛋白或纳米颗粒与内皮表面负电成分之间的静电相互作用,从而提高内吞和跨胞转运的机会[4,5]。那针对这些BBB穿梭机制,目前都有哪些热门靶点值得布局呢?
三、受体介导跨胞转运RMT靶点
如前所述,由于RMT机制天然适合搬运大分子货物,所以抗体、酶替代药物、双特异性抗体、融合蛋白乃至部分核酸偶联物,通常都会优先考虑RMT路径。目前热门的RMT靶点包括转铁蛋白受体1(TfR1)、胰岛素受体(INSR)、IGF1R、LRP1以及CD98hc,其中前几类代表“经典入口”,后者则代表“新一代入口”[5]。
3.1 TfR1:验证最充分的BBB穿梭靶点
TfR1由TFRC基因编码,是目前BBB递送领域最热门,同时也是最重要的靶点。它之所以重要,不单是因为在脑内皮表面表达较高,更是因为它已经积累了从概念验证到临床应用的成功经验。JCR的pabinafusp alfa就是借助transferrin receptor-mediated transcytosis 实现跨BBB 递送的代表产品;Roche的trontinemab同样体现了TfR1 shuttle思路在阿尔茨海默病方向的持续推进[1,3]。这意味着TfR1的价值已经不只是一个好用的受体,而是一种被行业重复验证过的开发范式。
而且,TfR1路线也最能说明BBB递送不是简单的“绑上去就能过”。Bien-Ly等人的经典研究表明,TfR抗体的脑摄取效率与其受体亲和力、价态以及胞内转运命运密切相关;高亲和力并不一定带来更好的脑递送,反而可能导致受体下调、胞内滞留或更强的溶酶体分选[6]。相关综述也持续强调,TfR1介导BBB转运的成败,高度依赖抗体形式、结合表位、受体占用程度和剂量区间[5]。
3.2 CD98hc:正在崛起的新一代大分子递送入口
除开TfR1,CD98hc由SLC3A2基因编码,是近两年热度上升最快的BBB 点之一。Chew等人在Nature Communications发表的研究显示,靶向CD98hc的transport vehicle能在人源化小鼠和食蟹猴中实现差异化的脑递送,其动力学表现与TfR平台不同,特点是脑内暴露更慢、更持久,并具有独特的脑内分布和安全性特征[7]。这说明CD98hc并不是简单的与TfR1相似的另一个靶点,而更可能是代表另一类适合持久脑暴露或特定药物负载形式的入口。对于需要更长脑内停留时间的抗体、酶或其他生物大分子,CD98hc很可能会成为下一阶段平台竞争的关键分流口[7]。
3.3 IGF1R/INSR:生理相关性更强,但转化门槛更高
IGF1R和INSR也是RMT领域反复被提到的候选受体。它们的吸引力在于本身就参与脑内营养与生长信号调控,理论上具备天然的跨屏障运输相关性。Shin等人在Cell Reports Methods中报道的IGF1R-based shuttle“Grabody B”表明,非中和型IGF1R抗体可以作为安全且有效的分子穿梭系统,将生物大分子递送至脑内[8]。这提示IGF1R并非仅仅是一个的替补靶点,而是真正具备独立平台潜力的BBB入口。
但从开发难度看,IGF1R和INSR通常比TfR1更敏感。原因在于它们与全身代谢、生长调控和外周组织分布的关系更紧密,因此安全窗口、物种差异和外周干扰问题都更难处理[5]。换句话说,这类受体的吸引力在于生理相关性强,而挑战也恰恰来自这种生理相关性。
四、转运体介导运输CMT靶点
如前所述,CMT更适合小分子、前药和结构伪装策略。对这一路径而言,决定成败的重点不是抗体工程,而是分子结构是否能被转运体识别、结合和转运[4,9]。目前热门的CMT靶点L型氨基酸转运体1(LAT1)、葡萄糖转运蛋白1(GLUT1)、有机阴离子转运多肽(OATP)、单羧酸转运体(MCT)等。
4.1. LAT1
在BBB小分子递送领域,LAT1几乎是最经典的入口之一。Puris等人的综述指出,LAT1一直是最广泛研究的药物递送转运体之一,已经被广泛用于跨生物屏障的药物递送研究[10]。而且,LAT1并不是停留在理论层面的靶点,它与多种已知CNS活性分子的递送逻辑直接相关,L-DOPA、gabapentin、pregabalin等都常被视作利用大中性氨基酸转运体系进入中枢的代表案例[10]。这意味着对于药化团队而言,LAT1的价值在于,它把脑递送问题从复杂载体系统,转化为更可控的结构设计问题。
同时,LAT1也非常适合前药化策略。只要药物在保留有效药效的同时满足LAT1的识别偏好,就有机会提升BBB穿透能力和脑内暴露。因此,LAT1 并不只是一个“运输蛋白”,而是小分子中枢药物优化中最值得持续工程化的分子入口之一[9,10]。
4.2 GLUT1
GLUT1又称为SLC2A1,是BBB上最关键的葡萄糖转运蛋白之一,对维持脑能量供应具有基础性作用。围绕 BBB葡萄糖代谢与脑健康的最新综述指出,GLUT1在脑微血管内皮中的功能对于维持BBB正常状态和脑葡萄糖供应至关重要[11]。这也解释了为什么GLUT1长期被视为极具吸引力的脑递送靶点:如果能够合理利用这一入口,理论上就有机会通过糖基化前药或糖修饰递送系统提高脑摄取。
但GLUT1的问题在于,它不是富余通道,而是脑能量代谢的基础设施。任何以GLUT1为入口的药物设计,都必须避免与生理葡萄糖转运发生强竞争,否则即使脑递送效率有所提升,也可能付出代谢稳定性和安全性上的代价[11]。因此,GLUT1更适合作为高约束条件下的精细化开发靶点,而不适合被简单理解为另一个可借用的通道。
4.3 OATP、MCT等摄取转运体
除了LAT1和GLUT1,BBB上还存在OATP、MCT等多类摄取型转运系统。Ronaldson和Davis 的综述明确提出,BBB uptake transporters代表了优化脑递送的重要机会,因为它们能够利用内源性生物学过程促进脑内药物累积[9]。不过,相比LAT1这类已有较成熟开发经验的入口,OATP和MCT更像是场景化靶点:它们往往更适合特定病理状态、特定底物结构或特定药物类型,而不一定适合做成高度通用的平台[4,9]。
五、吸附介导跨胞转运AMT靶点
如前所述,AMT更多是基于分子性质或电荷特征的策略型路径,而不是像像TfR1、CD98hc或LAT1那样典型的受体驱动型靶点赛道。AMT 的优点是对cargo的包容度较高,不一定依赖某一个高表达受体;但它的短板也很明显,那就是特异性通常较弱、外周组织的非特异分布更难控制[4,5]。AMT目前没有公认的一线靶点,不过从研究与应用热度来看,硫酸乙酰肝素蛋白聚糖(HSPGs)算得上是AMT里最接近靶点化的一类蛋白,比如Syndecan、Glypican家族,可通过带正电的分子(CPP、多肽、纳米颗粒)与细胞表面负电荷糖胺聚糖结合,触发内吞/跨胞转运。
六、缔码生物现货抗体分子助力BBB药物开发
围绕血脑屏障穿梭中最具转化价值的入口分子,优质抗体资源正成为推动项目快速落地的关键一环。缔码生物已针对主流RMT与CMT路径完成布局,提供覆盖TFRC/TfR1、CD98/SLC3A2以及GLUT1/SLC2A1等核心靶点的现货抗体分子,可直接用于脑穿梭抗体设计与功能验证,显著缩短早期研发周期。除了现货抗体分子,缔码生物还提供高品质的药物靶点重组蛋白与流式抗体,其中重组蛋白包括胞外域(ECD)蛋白及全长多跨膜蛋白,涵盖多种属、多标签及Biotin标记等,更多产品详情,欢迎垂询。

参考文献:
- Roche. Roche presents new insights in Alzheimer’s disease research across its diagnostics and pharmaceutical portfolios at AAIC. 2025.
- AbbVie. AbbVie Completes Acquisition of Aliada Therapeutics. 2024.
- JCR Pharmaceuticals. JCR Pharmaceuticals Announces Approval of IZCARGO® for Treatment of MPS II in Japan. 2021.
- Ding L, Kshirsagar P, Agrawal P, et al. Crossing the Blood-Brain Barrier: Innovations in Receptor- and Transporter-Mediated Transcytosis Strategies. Pharmaceutics. 2025;17(6):706.
- Haqqani AS, Bélanger K, Stanimirovic DB. Receptor-mediated transcytosis for brain delivery of therapeutics: receptor classes and criteria. Frontiers in Drug Delivery. 2024;4:1360302.
- Bien-Ly N, Yu YJ, Bumbaca D, et al. Transferrin receptor trafficking determines brain uptake of TfR antibody affinity variants. Journal of Experimental Medicine. 2014;211(2):233-244.
- Chew KS, Wells RC, Moshkforoush A, et al. CD98hc is a target for brain delivery of biotherapeutics. Nature Communications. 2023;14:5053.
- Shin JW, An S, Kim D, et al. Grabody B, an IGF1 receptor-based shuttle, mediates efficient delivery of biologics across the blood-brain barrier. Cell Reports Methods. 2022;2(11):100338.
- Ronaldson PT, Davis TP. Blood-brain barrier transporters: a translational consideration for CNS delivery of neurotherapeutics. Expert Opinion on Drug Delivery. 2024;21(1):71-89.
- Puris E, Gynther M, Auriola S, Huttunen KM. L-Type amino acid transporter 1 as a target for drug delivery. Pharmaceutical Research. 2020;37:88.
- Zhu Y, Verkhratsky A, Chen H, Yi C. Understanding glucose metabolism and insulin action at the blood-brain barrier: Implications for brain health and neurodegenerative diseases. Acta Physiologica. 2025;241(2):e14283.


